题目内容
X2-的核外电子排布为2、8、8,则X元素在周期表中的位置是
| A.第三周期0族 | B.第三周期VIA族 |
| C.第三周期VIIA族 | D.第四周期IA族 |
B
解析试题分析:X2-的核外电子排布为2、8、8,说明X原子的核外电子数是16,为硫元素,位于元素周期表的第三周期VIA族,答案选B。
考点:考查原子结构与在元素周期表中位置的关系

练习册系列答案
相关题目
在短周期元素中,原子最外电子层只有1个或2个电子的元素是( )
| A.金属元素 | B.稀有气体元素 | C.非金属元素 | D.无法确定为哪一类元素 |
已知1~18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同的电子层结构,下列关系正确的是
| A.质子数:c>b | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
放射性同位素电池采用的放射性同位素主要有90 38Sr等。下列关于90 38Sr的说法正确的是
| A.质子数为90 | B.中子数为38 | C.电子数为52 | D.质量数为90 |
有X,Y两种原子,X原子的M电子层比Y原子的M电子层少3个电子,Y原子的L电子层的电子数恰为X原子的L层电子数的2倍,则X,Y元素的元素符号分别为
| A.Mg和S | B.N和Be | C.Si和B | D.C和Al |
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是 ( )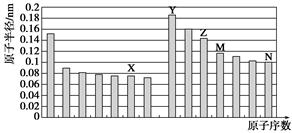
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的沸点相比,前者较低 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
(双选)已知铍(Be)的原子序数为4。下列对铍及其化合物的叙述中,正确的是( )。
| A.铍的原子半径大于硼的原子半径 |
| B.氯化铍难溶于水 |
| C.氢氧化铍的碱性比氢氧化钙的弱 |
| D.单质铍跟冷水反应迅速产生氢气 |
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是( )
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |