题目内容
知反应:A(g)+B(g)=C(g)+D(g)的能量变化如图所示,下列说法正确的是
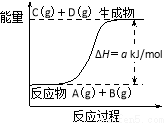
A.若此反应过程中有电子转移,可设计成原电池
B.该反应为吸热反应
C.反应物的总能量高于生成物的总能量
D.该反应只有在加热条件下才能进行
B
【解析】
试题分析:A、该反应是吸热反应,不是自发的氧化还原反应,不能设计成原电池,错误;B、该反应的反应物的总能量低于生成物的总能量,是吸热反应,正确;C、该反应的反应物的总能量低于生成物的总能量,错误;D、吸热反应不一定需要加热条件,放热反应不一定不需要加热条件,反应的热效应与反应条件无关,错误,答案选B。
考点:考查对化学反应热效应的判断

 单元期中期末卷系列答案
单元期中期末卷系列答案(共11分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 |
|
|
| ① | ② | ③ |
|
|
3 | ④ |
| ⑤ |
|
| ⑥ | ⑦ | ⑧ |
4 | ⑨ |
|
|
|
|
| ⑩ |
|
(1) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是: ,
碱性最强的化合物的电子式是: 。
(2) 最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式 。
(3) 用电子式表示元素④与⑥的化合物的形成过程: ,
该化合物属于 (填 “共价”或“离子”)化合物。
(4)表示①与⑦的化合物的电子式 ,该化合物是由 (填“极性”“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_____________________
(要求用离子符号表示)。
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为: 。
(7)写出⑥的最高价氧化物的水化物和①的单质反应的化学方程式: 。

 cC(g)+dD(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍。下列叙述正确的是( )
cC(g)+dD(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍。下列叙述正确的是( ) 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是 。
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是 。