题目内容
(11分)地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面是海水资源综合利用的部分流程图,请根据该图回答下列问题:

(1)淡化海水的方法有__________________(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO2-4等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________(填化学式),之后________(填操作名称),再加入适量________(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)反应④由无水MgCl2制取金属镁的常用工业方法是__________________。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是_________________________。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式__________________________________。最后再用H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________________________。
本题共11分。方程式未配平扣1分
(1)蒸馏法(1分); Na2CO3(1分); 过滤(1分); 盐酸(1分)
(2)电解法(1分)
(3)SO2>Br->Cl-(2分)
(4)3CO2-3+3Br2=5Br-+BrO-3+3CO2↑(2分);
5Br-+BrO3-+6H+=3Br2+3H2O(2分)
【解析】
试题分析:(1)海水淡化即是使海水中的金属阳离子浓度降低,可采用蒸馏的方法、电渗析法、沉淀法等;除去粗盐中含有Ca2+、Mg2+、SO2-4等离子,加入氢氧化钠溶液除去Mg2+,少量的Ca2+,加入BaCl2溶液除去SO2-4,然后溶液中多余的Ba2+用碳酸钠溶液除去,所以应再加入Na2CO3溶液,过滤后再加入适量的稀盐酸除去碳酸根离子即可;
(2)由无水氯化镁制取镁的方法通常用电解法得到单质镁;
(3)根据氧化还原反应中的氧化性、还原性的判断规律可知,Cl2置换出Br2,说明溴离子的还原性大于氯离子,再用空气吹出溴并用SO2吸收,转化为Br-,说明二氧化硫的还原性大于溴离子,所以Cl-、SO2、Br-还原性由强到弱的顺序是SO2>Br->Cl-;
(4)用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,根据题意写出离子方程式为
3CO2-3+3Br2=5Br-+BrO-3+3CO2↑;再用H2SO4处理所得溶液重新得到Br2,在酸性条件下Br-、BrO-3发生氧化还原反应生成溴单质和水,离子方程式为5Br-+BrO3-+6H+=3Br2+3H2O。
考点:考查海水淡化的方法,离子方程式的书写,氧化还原反应规律的应用

 2NaOH+H2↑
2NaOH+H2↑ 
 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )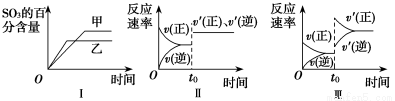
 NH3↑+H2O
NH3↑+H2O