题目内容
13.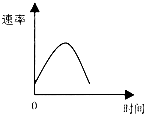 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度.
| A. | ①④ | B. | ③④ | C. | ①②③ | D. | ②③ |
分析 由图可知,该反应速率先增大后减小,结合温度、浓度对反应速率的影响解答.
解答 解:由图可知,该反应速率先增大后减小,
该反应为放热反应,放出热量,温度升高,则反应速率加快,
后来盐酸浓度减小,则反应速率逐渐减小,
另外由反应可知Mg参加反应,开始接触面积大,反应速率快,但随反应的进行,接触面积减小,则反应速率减小,
则影响因素主要为①②③,
故选:C.
点评 本题考查影响化学反应速率的因素,注意把握浓度、温度对反应速率的影响即可解答,注重基础知识的考查,注意图象分析与反应特点的应用,题目难度不大.

练习册系列答案
相关题目
3.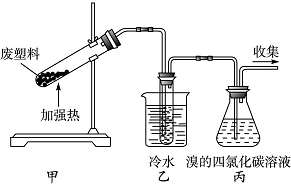 加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯.用如图所示装置探究废旧塑料的再利用.下列叙述中不正确的是( )
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯.用如图所示装置探究废旧塑料的再利用.下列叙述中不正确的是( )
 加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯.用如图所示装置探究废旧塑料的再利用.下列叙述中不正确的是( )
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯.用如图所示装置探究废旧塑料的再利用.下列叙述中不正确的是( )| A. | 该实验是聚丙烯的发生加聚反应的实验 | |
| B. | 装置乙的试管中可收集到芳香烃 | |
| C. | 装置丙中的试剂可吸收烯烃以制取卤代烃 | |
| D. | 最后收集的气体可作燃料 |
4.有下列两组命题
B组中命题正确,且能用A组命题加以正确解释的是( )
| A组 | B组 |
| Ⅰ.H2O分子间存在氢键,H2S则无 | ①H2O比H2S稳定 |
| Ⅱ.晶格能NaI比NaCl小 | ②NaCl比NaI熔点高 |
| Ⅲ.晶体类型不同 | ③N2分子比磷的单质稳定 |
| Ⅳ.元素第一电离能大小与原子外围电子排布有关,不一定像电负性随原子序数递增而增大 | ④同周期元素第一电离能大的,电负性不一定大 |
| A. | Ⅰ① | B. | Ⅱ② | C. | Ⅲ③ | D. | Ⅳ④ |
1.下列物质①HCl溶液 ②H2O ③C2H5OH 都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
| A. | ①>②>③ | B. | ②>①>③ | C. | ③>①>② | D. | ②>③>① |
8. H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
 H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
18.在带有活塞的密闭容器中发生反应:Fe2O3+3H2═2Fe+3H2O,采取下列措施不能改变反应速率的是( )
| A. | 加热 | B. | 保持容器体积不变,增加H2输入量 | ||
| C. | 充入N2,保持容器内压强不变 | D. | 充入N2,保持容器体积不变 |
5.如图为铜锌原电池示意图,下列说法正确的是( )
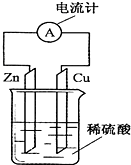

| A. | 锌片上有气泡产生 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电流由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
2.下列实验装置能达到实验目的,且实验装置无明显错误的是(夹持仪器未画出)( )
| A. | 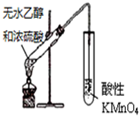 A装置用于检验乙醇发生消去反应的产物 | |
| B. | 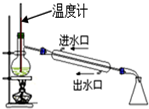 B装置可用于分离乙醇和丙三醇形成的混合物 | |
| C. | 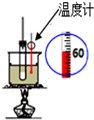 C装置用于实验室制硝基苯 | |
| D. | 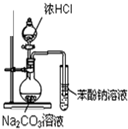 D装置可证明酸性:盐酸>碳酸>苯酚 |
3.分子式为C7H14O2的有机物Q,在稀硫酸溶液加热可转化为乙醇与另一种酸性物质,则Q的结构最多有( )
| A. | 6种 | B. | 4种 | C. | 3种 | D. | 2种 |