题目内容
2.某元素的一个原子形成的离子可表示为baXn-,下列说法中正确的是(NA表示阿伏伽德罗常数)( )| A. | baXn-中含有的中子数为a+b | B. | baXn-中含有的电子数为a-n | ||
| C. | X原子的质量约为(b/NA)g | D. | 此元素的相对原子质量为b |
分析 baXn-中质子数是a,质量数是b,中子数=质量数-质子数,阴离子中核外电子数=核内质子数+电荷数,元素的相对原子质量不等于原子的质量数.
解答 解:A、该微粒中中子数=质量数-质子数=b-a,故A错误.
B、该微粒的核外电子数=核内质子数+电荷数=a+n,故B错误.
C、原子的质量为原子的相对原子质量和阿伏伽德罗常数的比值,即X原子的质量约为(b/NA)g,故C正确.
D、元素的相对原子质量不等于原子的质量数,故D错误.
故选C.
点评 本题考查了质子数、质量数和中子数之间的关系,难度不大,明确阴阳离子核外电子数的计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列实验装置或操作正确的是( )
| A. |  从碘水中分离出碘 | B. |  检验试液中NH${\;}_{4}^{+}$的存在 | ||
| C. |  干燥SO2气体 | D. |  收集HCl气体 |
11.如图所示的装置,C.D.E.F.X.Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )
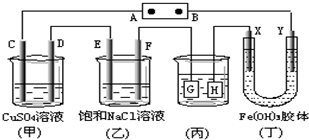

| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |



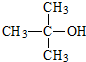
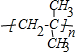
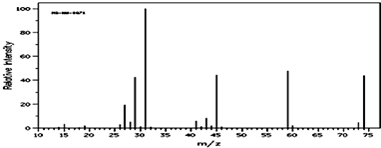



 的加成类似于
的加成类似于 的加成)
的加成) .
. .
. .
.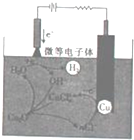 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题: