题目内容
化合物A(C11H12O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B (C2H4O2)和C.请回答下列问题:
(1)B分子中只有一个官能团.则B的结构简式是
(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,则C的结构简式是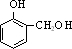
 ;写出C与溴水反应的化学方程式
;写出C与溴水反应的化学方程式
 .
.
(1)B分子中只有一个官能团.则B的结构简式是
CH3COOH
CH3COOH
,B与甲醇在浓硫酸作用下加热反应生成D,该反应的化学方程式是CH3COOH+CH3OH
CH3COOCH3+H2O
| 浓硫酸 |
| △ |
CH3COOH+CH3OH
CH3COOCH3+H2O
;写出能发生银镜反应的B的同分异构体的结构简式| 浓硫酸 |
| △ |
HCOOCH3或HOCH2CHO
HCOOCH3或HOCH2CHO
;(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,则C的结构简式是




分析:(1)化合物A(C11H12O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B (C2H4O2)和C,B分子中只有一个官能团,所以B是乙酸,与甲醇在浓硫酸作用下加热反应生成乙酸甲酯,能发生银镜反应的B的同分异构体应含有醛基;
(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,根据A中O原子数目可知应含有2个酯基,C中应含有2个-OH,则A水解生成2个B分子和1个C分子,因A的分子式为C11H12O4,则C11H12O4+2H2O→2C2H4O2+C,C的分子式为C7H8O2,则C应为 ,含有酚羟基,可与溴水发生取代反应.
,含有酚羟基,可与溴水发生取代反应.
(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,根据A中O原子数目可知应含有2个酯基,C中应含有2个-OH,则A水解生成2个B分子和1个C分子,因A的分子式为C11H12O4,则C11H12O4+2H2O→2C2H4O2+C,C的分子式为C7H8O2,则C应为
 ,含有酚羟基,可与溴水发生取代反应.
,含有酚羟基,可与溴水发生取代反应.解答:解:(1)化合物A(C11H12O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B (C2H4O2)和C,B分子中只有一个官能团,所以B是乙酸,结构简式为CH3COOH,与甲醇在浓硫酸作用下加热反应生成乙酸甲酯,反应的方程式为CH3COOH+CH3OH
CH3COOCH3+H2O,
B的同分异构体能发生银镜反应,应含有醛基,则可为HCOOCH3或HOCH2CHO,
故答案为:CH3COOH;CH3COOH+CH3OH
CH3COOCH3+H2O;HCOOCH3或HOCH2CHO;
(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,根据A中O原子数目可知应含有2个酯基,C中应含有2个-OH,则A水解生成2个B分子和1个C分子,因A的分子式为C11H12O4,
则C11H12O4+2H2O→2C2H4O2+C,C的分子式为C7H8O2,则C应为 ,含有酚羟基,可与溴水发生取代反应,酚羟基的邻位和对位分别有1个H可被取代,则反应的方程式为
,含有酚羟基,可与溴水发生取代反应,酚羟基的邻位和对位分别有1个H可被取代,则反应的方程式为 ,
,
故答案为: ;
; .
.
| 浓硫酸 |
| △ |
B的同分异构体能发生银镜反应,应含有醛基,则可为HCOOCH3或HOCH2CHO,
故答案为:CH3COOH;CH3COOH+CH3OH
| 浓硫酸 |
| △ |
(2)若A中官能团只有酯基,C为邻位有2个侧链的芳香族化合物,根据A中O原子数目可知应含有2个酯基,C中应含有2个-OH,则A水解生成2个B分子和1个C分子,因A的分子式为C11H12O4,
则C11H12O4+2H2O→2C2H4O2+C,C的分子式为C7H8O2,则C应为
 ,含有酚羟基,可与溴水发生取代反应,酚羟基的邻位和对位分别有1个H可被取代,则反应的方程式为
,含有酚羟基,可与溴水发生取代反应,酚羟基的邻位和对位分别有1个H可被取代,则反应的方程式为 ,
,故答案为:
 ;
; .
.点评:本题考查有机物的推断,为高考常见题型,侧重于考查学生综合运用化学知识的能力和分析问题的能力,根据题给信息正确推断C的结构简式为解答该题的关键,注意把握有机物官能团的性质,题目难度中等.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目








 三种基团,无环状结构,三种基团的数目关系为n3=
三种基团,无环状结构,三种基团的数目关系为n3=