题目内容
12.在玻璃熔炉中,纯碱与石英反应生成Na2SiO3和CO2.下列说法正确的是( )| A. | 该反应是氧化还原反应 | B. | 微粒的半径:r(Si)>r(Na) | ||
| C. | 硅酸的酸性强于碳酸 | D. | Na2CO3中含有离子键和共价键 |
分析 A、无元素化合价的变化;
B、同周期从左到右半径逐渐减小;
C、非金属性越强最高价氧化物对应水化物的酸性越强;
D、碳酸钠中既含离子键又含共价键;
解答 解:A、无元素化合价的变化,所以该反应不是氧化还原反应,故A错误;
B、同周期从左到右半径逐渐减小,所以微粒的半径:r(Si)<r(Na),故B错误;
C、非金属性越强最高价氧化物对应水化物的酸性越强,非金属性C>Si,所以硅酸的酸性强于碳酸,故C错误;
D、碳酸钠中既含离子键又含共价键,所以Na2CO3中既含有离子键又含共价键,故D正确;
故选D.
点评 本题考查硅及硅的化合物的相关知识,涉及氧化还原反应、微粒半径的大小、酸性强弱和化学键的类型,比较容易.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
2.实验室从含溴化氢的废液中提取溴单质,下列步骤中的实验装置正确的是( )
| A. | 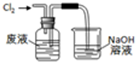 氧化废液中的溴化氢 | B. |  分离CCl4层和水层 | ||
| C. | 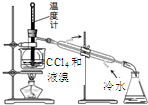 分离四氯化碳和液溴 | D. | 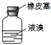 储存液溴 |
3.β-月桂烯的结构如图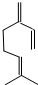 所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
 所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
17.一种氢气-磷酸燃料电池的原理示意如图.下列有关该电池的说法正确的是( )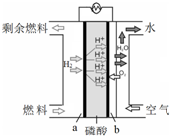

| A. | b极发生还原反应 | |
| B. | a极的反应式:H2+2OH--2e-═2H2O | |
| C. | 放电时,电子从b极经外电路流向a极 | |
| D. | 电池工作一段时间后,溶液中磷酸的浓度会升高 |
1.将H(CB11H6Cl6)与C60反应,C60得到一个质子,制得离子化合物[HC60]+[CB11H6Cl6]-.下列反应中,反应类型与之相似的是( )
| A. | Mg+2HCl→MgCl2+H2↑ | B. | NaOH+HCl→NaCl+H2O | ||
| C. | H2O+CH3COOH?H3O++CH3COO- | D. | NH3+HCl→NH4Cl |
2.分析如下残缺的反应:RO3-+□+6H+→3R2↑+3H2O.下列叙述正确的是( )
| A. | 上式中缺项所填物质在反应中作氧化剂 | |
| B. | 在RO3-参与的氧化还原反应中,R元素只能被还原 | |
| C. | 上述反应中,转移电子数为5NA | |
| D. | 同周期主族元素原子中R的原子半径最小 |
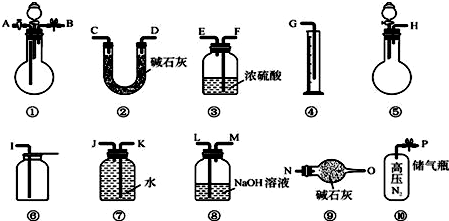
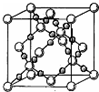 X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.
X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.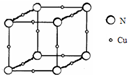 原子序数依次增大的X、Y、Z、W四种元素,X、Z基态原子的2p原子轨道上均有2个未成对电子,W基态原子的除第四层只有1个电子外,其余内层均为全满结构.
原子序数依次增大的X、Y、Z、W四种元素,X、Z基态原子的2p原子轨道上均有2个未成对电子,W基态原子的除第四层只有1个电子外,其余内层均为全满结构.