题目内容
 在30℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,经过10s达到平衡,浓度变化曲线如图所示,试回答:
在30℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,经过10s达到平衡,浓度变化曲线如图所示,试回答:(1)在上述条件下,从反应开始直至10s时,二氧化氮的平均反应速率为
(2)30℃时,反应2NO2?N2O4的平衡常数的值为
(3)若保持20s时的温度和压强不变,再向平衡混合气中充入0.075molN2O4,在第30s时重新达到平衡,则第30s时平衡混合气的体积为
(4)若保持温度不变,在第20s再向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L试通过计算确定平衡移动的方向.
分析:(1)根据公式反应速率v=
来计算;
(2)根据图象中平衡时各物质的浓度,结合平衡常数K=
求算;该反应正方向为放热反应,据此判断温度对K的影响;
(3)保持相同温度和压强情况下,再充入0.075 molN2O4达新平衡与原平衡等效,将N2O4全部转化为NO2,再根据物质的量之比等于体积比计算;根据20s时气体总物质的量为(0.1mol/L+0.05mol/L)×2L=0.3mol,加入N2O4后气体总物质的量为0.3mol+0.075mol=0.375mol,根据物质的量之比等于体积比计算出容器体积,再求出加入N2O4后两种气体各自的浓度,30s达新平衡与原平衡等效,故c(NO2) c(N2O4)与原平衡相同,据此作图;
(4)扩大容器体积,则反应物所占体系压强减小,根据压强对平衡的影响判断.
| △c |
| t |
(2)根据图象中平衡时各物质的浓度,结合平衡常数K=
| [N2O4] |
| [NO2]2 |
(3)保持相同温度和压强情况下,再充入0.075 molN2O4达新平衡与原平衡等效,将N2O4全部转化为NO2,再根据物质的量之比等于体积比计算;根据20s时气体总物质的量为(0.1mol/L+0.05mol/L)×2L=0.3mol,加入N2O4后气体总物质的量为0.3mol+0.075mol=0.375mol,根据物质的量之比等于体积比计算出容器体积,再求出加入N2O4后两种气体各自的浓度,30s达新平衡与原平衡等效,故c(NO2) c(N2O4)与原平衡相同,据此作图;
(4)扩大容器体积,则反应物所占体系压强减小,根据压强对平衡的影响判断.
解答:解:(1)由图象可知10s时达到平衡状态,此时NO2浓度为0.10mol/L,所以NO2的浓度变化为△c(NO2)=0.20mol/L-0.10mol/L=0.10mol/L,
则其反应速率为:v=
=
=0.01 mol/(L?s);
故答案为:0.01 mol/(L?s);
(2)根据图象可知平衡时各物质的浓度为c(NO2)=0.10mol/L,c(N2O4)=0.05mol/L,则平衡常数K=
=
=5;已知该反应正方向为放热反应,升高温度平衡逆向移动,平衡常数减小,
故答案为:5;减小;
(3)保持相同温度和压强情况下,再充入0.075 molN2O4达新平衡与原平衡等效,则将N2O4全部转化为NO2,
由物质的量之比等于体积比得:
=
,解得V=2.75L;
起点:20s时气体总物质的量为(0.1mol/L+0.05mol/L)×2L=0.3mol,加入N2O4后气体总物质的量为0.3mol+0.075mol=0.375mol,
在20s时加入N2O4后,体系体积:
=
,解得:V1=2.5L,故20s时c(NO2)=
=0.080mol/L,
c(N2O4)=
=0.070mol/L;
平衡点:30s达新平衡与原平衡等效,故c(NO2) c(N2O4)与原平衡相同,依此作图为: ;
;
故答案为:2.75L; ;
;
(4)通入He与反应无关,但是扩大容器体积,则反应物所占体系压强减小,平衡向着计量数增大的方向移动,即向逆方向移动,
故答案为:向逆方向移动.
则其反应速率为:v=
| △c |
| t |
| 0.10mol/L |
| 10s |
故答案为:0.01 mol/(L?s);
(2)根据图象可知平衡时各物质的浓度为c(NO2)=0.10mol/L,c(N2O4)=0.05mol/L,则平衡常数K=
| [N2O4] |
| [NO2]2 |
| 0.05 |
| 0.12 |
故答案为:5;减小;
(3)保持相同温度和压强情况下,再充入0.075 molN2O4达新平衡与原平衡等效,则将N2O4全部转化为NO2,
由物质的量之比等于体积比得:
| 0.40mol |
| 2L |
| (0.40+0.075×2)mol |
| V |
起点:20s时气体总物质的量为(0.1mol/L+0.05mol/L)×2L=0.3mol,加入N2O4后气体总物质的量为0.3mol+0.075mol=0.375mol,
在20s时加入N2O4后,体系体积:
| 0.30mol |
| 2L |
| (0.30+0.075)mol |
| V1 |
| 0.20mol |
| 2.5L |
c(N2O4)=
| 0.175 mol |
| 2.5L |
平衡点:30s达新平衡与原平衡等效,故c(NO2) c(N2O4)与原平衡相同,依此作图为:
 ;
;故答案为:2.75L;
 ;
;(4)通入He与反应无关,但是扩大容器体积,则反应物所占体系压强减小,平衡向着计量数增大的方向移动,即向逆方向移动,
故答案为:向逆方向移动.
点评:本题考查了反应速率和化学平衡的有关计算和图象,影响平衡的因素,及等效平衡原理的应用等,题目难度较大.

练习册系列答案
相关题目
I.在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)表中b______c(填“<”、“=”、“>”).0~20s内N2O4的平均反应速率为______.
(2)80℃时,该反应的平衡常数K=______.
(3)在其他条件相同时,该反应的K值越大,表明建立平衡时______.
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2有浓度之比越大D.正反应进行的程度越大
(4)要增大该反应的K值,可采取的措施______.
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂D.升高温度
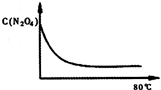
(5)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.

| 时间/s c/mol?L-1 | 20 | 40 | 60 | 80 | 100 | |
| N2O4 | 0.20 | a | 0.10 | c | d | e |
| NO2 | 0.12 | b | 0.26 | 0.30 | 0.30 |
(1)表中b______c(填“<”、“=”、“>”).0~20s内N2O4的平均反应速率为______.
(2)80℃时,该反应的平衡常数K=______.
(3)在其他条件相同时,该反应的K值越大,表明建立平衡时______.
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2有浓度之比越大D.正反应进行的程度越大
(4)要增大该反应的K值,可采取的措施______.
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂D.升高温度
(5)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.