题目内容
14.下列物质属于离子化合物的是( )| A. | NH3 | B. | CO2 | C. | HCI | D. | NaCl |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,以此来解答.
解答 解:A.NH3只含共价键,为共价化合物,故A不选;
B.CO2中只含共价键,为共价化合物,故B不选;
C.HCl只含共价键,为共价化合物,故C不选;
D.NaCl含离子键,为离子化合物,故D选;
故选D.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
相关题目
9.能说明氯元素的非金属性比硫元素强的事实是( )
①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸.
①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸.
| A. | ①④ | B. | ①② | C. | ③④ | D. | ②④ |
6.下列关于有机物的说法正确的是( )
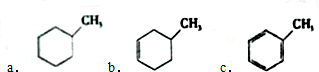
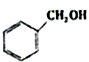
| A. | 乙醛和甲苯都能与溴水反应 | |
| B. | 蛋白质和油脂都属于天然高分子化合物 | |
| C. | 甲烷中混有的乙烯可通过溴的四氯化碳除去 | |
| D. | 苯酚能使酸性高锰酸钾溶液褪色 |
3. 表是元素周期表的前三周期:
表是元素周期表的前三周期:
回答下列问题:
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是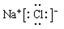 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
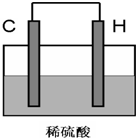
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.
 表是元素周期表的前三周期:
表是元素周期表的前三周期:| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | A | |||||||
| 二 | B | C | D | E | F | |||
| 三 | G | H | I | J |
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是
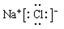 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.


 c.
c.