题目内容
某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
|
时间/s |
0 |
5 |
10 |
15 |
|
读数/g |
215.2 |
211.4 |
208.6 |
208.6 |
请你据此分析计算:
(1)实验中产生的CO2气体质量为 ;
(2)该产品中碳酸钠的质量分数 (结果精确到小数点后一位) 。
(1) 6.6克 [2分,未写单位扣1分] (2) 96.4% [3分]
【解析】
试题分析:(1)根据比值数据可知,反应进行到10s时,气体的物质的量不再发生变化,所以CO2的质量是208.6g-215.2g=6.6g。
(2)根据碳原子守恒可知,碳酸钠的质量是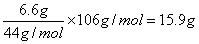 ,则该产品中碳酸钠的质量分数是
,则该产品中碳酸钠的质量分数是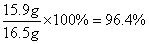
考点:考查碳酸钠和盐酸反应的有关计算
点评:该题是高考中的常见题型和考点,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和规范答题能力,提高学生灵活运用基础知识解决实际问题的能力。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案(5分)某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放人烧杯中,将烧杯放在电子称上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
| 时间/s | 0 | 5 | 10 | 15 |
| 读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
请你据此分析计算:
(1)该产品中碳酸钠的质量分数?(结果精确到0。l%)
(2)若反应后溶液为150.0 mL,计算溶液中NaCI物质的量浓度。
某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
| 时间/s | 0 | 5 | 10 | 15 |
| 读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
(1)实验中产生的CO2气体质量为 ;
(2)该产品中碳酸钠的质量分数 (结果精确到小数点后一位) 。
(5分)某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放人烧杯中,将烧杯放在电子称上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
|
时间/s |
0 |
5 |
10 |
15 |
|
读数/g |
215.2 |
211.4 |
208.6 |
208.6 |
请你据此分析计算:
(1)该产品中碳酸钠的质量分数?(结果精确到0。l%)
 (2)若反应后溶液为150.0 mL,计算溶液中NaCI物质的量浓度。
(2)若反应后溶液为150.0 mL,计算溶液中NaCI物质的量浓度。