��Ŀ����
��.ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϡ�
A����ȡ��Һ�� B������ C���ᾧ�� D����Һ�� E������ F�����˷�
��1�����뱥��ʳ��ˮ��ɳ�ӵĻ����
��2��������غ��Ȼ��ƵĻ����Һ�л�������
��3������ˮ�ͱ��Ļ����
��4���������Ȼ�̼���е�Ϊ76.75��C���ͼױ����е�Ϊ110.6��C������֪���Ȼ�̼�ͼױ����� ��
��.��1��ָ����ͼװ����A��B������

A B
��2����Һ�������õ�����Ҫ������ ��
��.��1��F ��2�� C ��3�� D ��4�� E
��.��1��A ������ƿB ������ ����2�� ��Һ©��
��������
�����������.��1������ʳ��ˮ��ɳ��Ϊ������Һ�岻���ܵĻ������ù��˵ķ������룬ѡF����2������ص��ܽ�����¶�Ӱ����Ȼ��Ƶ��ܽ�����¶�Ӱ�첻����������ȴ�ᾧ���ɷ��룬ѡC����3��ˮ�ͱ��ֲ㣬���÷�Һ©����Һ���ɣ�ѡD����4�����Ȼ�̼�ͼױ����������ڷе㲻ͬ��Һ�壬���Կ��Բ�������ķ������룬ѡE��
��. ��1��ͼװ��������װ�ã�A������������������ƿ��B�����������ܣ���2����Һ�������õ�����Ҫ�����Ƿ�Һ©����
���㣺�������ʵķ��롢�ᴿ�ͳ��ӡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�T1�¶��£���Ӧ2SO2(g)��O2(g)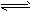 2SO3(g) ��H<0��ƽ�ⳣ��K=532.4��
2SO3(g) ��H<0��ƽ�ⳣ��K=532.4��
��1���÷�Ӧƽ�ⳣ���ı���ʽΪK= ��T1�¶��£�ijʱ�̲����ϵ�и�����Ũ�ȷֱ�Ϊc(SO2)=0.0600 mol��L��1��c(O2)=0.400 mol��L��1��c(SO3)=2.000mol��L��1����ʱ��Ӧ���еķ���Ϊ ��
��2���÷�Ӧ��S 0�������¶ȣ�ƽ�ⳣ�� ���������С�����䡱��
��3��T2�¶��£�2L�ݻ��̶��ļס������ܱ������з���������Ӧ�����ƽ��ʱ�й��������£�
���� | �� | �� |
��Ӧ��Ͷ���� | 2molSO2��1molO2 | 4molSO3 |
ƽ��ʱn(SO3)/mol | 1 | m |
��Ӧ���ת���� | ?1 | ?2 |
��������˵��T2�¶��¼�������������Ӧ�Ѵﵽƽ��״̬���� ��
A.SO2��O2��SO3�����ʵ���Ũ��֮��Ϊ2:1:2
B.����������ѹǿ���ٱ仯
C.��λʱ����2v(SO2)����= v(O2)����
D.�����ڻ��������ܶȲ��ٱ仯
�ڷ������������ݣ�?1+?2 1(�>����=����<��)��T1 T2(�>����=����<��)��
��14�֣�2013��10��9�գ�2013��ŵ������ѧ��������������̫���������ۻ�ѧ��������������˹������˹̹����ѧ��������ѧ�����˶�����ά�غ��ϼ��ݴ�ѧ��ѧ������Ү����л��������ӻ�ѧ��ϵ����˶�߶�ģ�Ͷ����������λ��ѧ�ҵ��о��ɹ��Ѿ�Ӧ���ڷ���������ֲ��Ĺ�����õ��о��У����������Ż�����������ҩ���̫���ܵ�ص���ơ�
��1������β����������Ҫԭ��Ϊ��2NO(g) + 2CO(g) 2CO2(g)+ N2(g) ��H��0ͬһ�����¸÷�Ӧ����Ӧ��ƽ�ⳣ��ΪK1���淴Ӧ�ı���ʽƽ�ⳣ��ΪK2��K1��K2�Ĺ�ϵʽΪ ��
2CO2(g)+ N2(g) ��H��0ͬһ�����¸÷�Ӧ����Ӧ��ƽ�ⳣ��ΪK1���淴Ӧ�ı���ʽƽ�ⳣ��ΪK2��K1��K2�Ĺ�ϵʽΪ ��
��2�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬���� ������ţ���
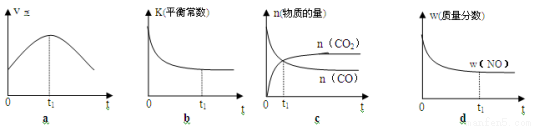
��3�������Ϊ10L���ܱ������У�����һ������CO2��H2����900��ʱ�������ȷ�Ӧ����¼ǰ5min�����ʵ�Ũ�ȣ���6min�ı��������������ʵ�Ũ�ȱ仯���±���
ʱ��/min | CO2��mol��L-1�� | H2��mol��L-1�� | CO��mol��L-1�� | H2O��mol��L-1�� |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
��ǰ2min����CO��ʾ�ĸû�ѧ��Ӧ������Ϊ ��
�ڵ�5��6min��ƽ���ƶ��Ŀ���ԭ���� ��
��4��ֱ���ŷ�úȼ�ղ������������������صĻ������⡣úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
��֪��CH4(g)+2NO2(g)��N2(g)��CO2(g)+2H2O(g) ��H����867 kJ��mol-1
2NO2(g)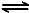 N2O4(g) ��H����56.9 kJ��mol-1
N2O4(g) ��H����56.9 kJ��mol-1
H2O(g) �� H2O(l) ��H �� ��44.0 kJ��mol-1
д��CH4����ԭN2O4(g)����N2��H2O(l)���Ȼ�ѧ����ʽ�� ��
��һ�������£�������NH3����NOx����֪NO��NH3������Ӧ����N2��H2O������NO��NH3�Ļ����1mol����ַ�Ӧ��õ��Ļ�ԭ��������������1.4 g����ԭ��Ӧ�������NO�����ʵ��������� mol
��6����һ�������£�Ҳ������H2����CO�ϳɼ״��Ͷ����ѣ�CH3OCH3���������������ʡ������������ʵ���1:1����Ӧ����ԭ�������ʴ�100%���ϳɵ����ʿ����� ��
a������ b���״� c����ȩ d������
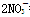 ===3Fe2����2NO����4H2O
===3Fe2����2NO����4H2O