��Ŀ����
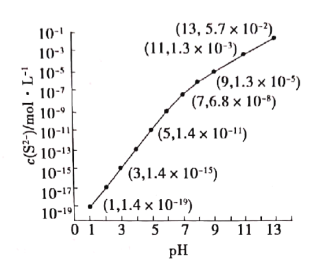
����Ŀ��25�棬��100mL0.1mol��L-1H2S��Һ�У�ͨ��HCl��������NaOH�����Ե�����ҺpH����ҺpH��c(S2-)��ϵ��ͼ��������Һ����ı仯��H2S�Ļӷ���������˵����ȷ���ǣ� ��
A.��c(H2S)+c(HS-)=0.043mol��L-1ʱ��pH=13
B.pH=1ʱ��c(H+)=c(Cl-)+c(HS-)+ c(S2-)+c(OH-)
C.�����Һ�м���NaOH����������ʱc(Na+)>c(HS-)>c(S2-)>c(H+)=c(OH-)
D.��֪��Ksp(MnS)=2.8��10-13��ij��Һ��amol��L-1Mn2+��0.10mol��L-1H2S������ҺpH=5ʱ��Mn2+��ʼ��������a=0.2
���𰸡�A
��������
A��c(H2S)+c(HS-)=0.043mol��L-1ʱ�����������غ���c(S2-)=0.1-0.043=0.057 mol��L-1����ͼ���֪��ʱpH=13��A��ȷ��
B��H2SΪ���ᣬ��pH=1ʱ��������ǿ���ʴ�ʱ��ͨ��HCl���壬��Һ�е�������ֻ��H+�����ݵ���غ�Ӧ��c(H+)=c(Cl-)+c(HS-)+ 2c(S2-)+c(OH-)��B����
C����Һ�����ԣ�����c(H+)=1��10-7mol/L������pH =7ʱ����ͼ��֪c(S2-)=6.8��10-8mol/L��c(H+)>c(S2-)��C����
D��pH=5ʱS2-��Ũ��Ϊ1.4��10-11mol/L����Qc=Ksp(MnS)ʱMn2+��ʼ����������c(Mn2+)=Ksp(MnS)/c(S2-)=2.8��1013��(1.4��10-11)=0.02mol /L����a-=0.02��D����
��ѡA��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�