题目内容
用下面两种方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入________.
(2)除去蒸馏水中溶解的O2常采用________的方法.
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是________.
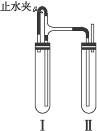
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备.

(1)在试管Ⅰ里加入的试剂是________.
(2)在试管Ⅱ里加入的试剂是________.
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________.
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是________.
解析:
|
答案:方法一 (1)稀H2SO4、铁屑 (2)煮沸 (3)使得Fe(OH)2能保存较长时间 方法二 (1)稀H2SO4、铁屑 (2)NaOH溶液 (3)检验试管Ⅱ出口处排出的氢气的纯度.当排出的H2纯净时,再夹紧止水夹 (4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入 解析:(1)Fe2+易水解,要加入稀H2SO4阻止其水解;易被空气中O2氧化,要加Fe粉,将被氧化的Fe3+还原成Fe2+. (2)气体的溶解度是随温度升高而降低的,所以煮沸后的水中溶解的O2变少. (3)两支试管,试管Ⅱ是开口式,无法用产生的气体将试液压入试管Ⅰ中,所以制取FeSO4应放在试管Ⅰ中,而在试管Ⅱ中盛不含O2的NaOH溶液.当Fe与稀H2SO4放入试管Ⅰ后,产生H2可从试管Ⅰ内短管处排出试管Ⅰ中的空气,经过止水夹通入试管Ⅱ中,再排尽试管Ⅱ中的空气.然后关闭止水夹,试管Ⅰ内产生的H2无法逸出,产生的H2气压将试管Ⅰ内FeSO4等溶液通过长导管压入试管Ⅱ内.在此压液过程中,液体处于H2气氛中,避免了空气中O2的氧化,使得Fe(OH)2能保存较长时间. |

 33、用下面两种方法可以制得白色的Fe(OH)2沉淀.
33、用下面两种方法可以制得白色的Fe(OH)2沉淀.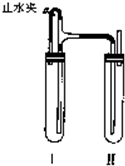 (2011?佛山二模)用下面两种方法可以制得白色的Fe(OH)2沉淀.
(2011?佛山二模)用下面两种方法可以制得白色的Fe(OH)2沉淀.