题目内容
4.下列有关物质检验的实验结论中正确的组合是( )| 实验操作 | 现象 | 实验结论 | |
| ① | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体一定是SO2 |
| ② | 将无色气体通入溴水中 | 溴水的黄色褪去 | 该气体可能是乙烯 |
| ③ | 向某溶液中滴入两滴KSCN溶液 | 溶液不显红色 | 该溶液一定含有Fe2+ |
| 另取该溶液少许,先滴入氯水,再 滴入KSCN溶液 | 溶液为红色 | ||
| ④ | 向某溶液中加入盐酸酸化的氯化钡 溶液 | 有白色沉淀产生 | 该溶液中可能含有SO42- |
| ⑤ | 将木炭和浓硫酸反应生成的气体通入 澄清石灰水中 | 有白色沉淀生成 | 该气体一定是CO2 |
| A. | ②④ | B. | ②③④ | C. | ①③⑤ | D. | ①②③④⑤ |
分析 ①能使品红溶液褪色的气体不一定是二氧化硫;
②能使溴水褪色的无色气体不一定是乙烯;
③铁离子和KSCN溶液反应生成血红色溶液,亚铁离子具有还原性,能被氯气氧化生成铁离子;
④能和盐酸酸化的氯化钡溶液反应生成白色沉淀的物质中可能含有硫酸根离子,也可能含有银离子;
⑤二氧化硫和二氧化碳都能和澄清石灰水反应生成白色沉淀.
解答 解:①能使品红溶液褪色的气体不一定是二氧化硫,氯气也能使品红溶液褪色,故错误;
②能使溴水褪色的无色气体不一定是乙烯,也可能是丙烯或乙炔等,故正确;
③铁离子和KSCN溶液反应生成血红色溶液,亚铁离子具有还原性,能被氯气氧化生成铁离子,向某溶液中滴入两滴KSCN溶液,溶液不显红色,说明不含铁离子;另取该溶液少许,先滴入氯水,再滴入KSCN溶液,溶液变红色,说明原来溶液中含有亚铁离子,故正确;
④能和盐酸酸化的氯化钡溶液反应生成白色沉淀的物质中可能含有硫酸根离子,也可能含有银离子,故正确;
⑤二氧化硫和二氧化碳都能和澄清石灰水反应生成白色沉淀,所以该气体可能是二氧化碳,故错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及元素化合物性质及离子检验,明确物质性质是解本题关键,知道常见离子的检验方法及实验现象,易错选项是⑤.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列反应的离子方程式书写正确的是( )
| A. | 二氧化硫通入溴水使其褪色 SO2+Br2+2H2O═4H++2Br-+SO32- | |
| B. | 石灰石与稀盐酸 CO32-+2H+═H2O+CO2↑ | |
| C. | 小苏打溶液中滴加醋酸溶液 HCO3-+CH3COOH=CH3COO-+H2O+CO2↑ | |
| D. | 氯化铝溶液中加入过量的氨水 Al3++4 NH3•H2O=4NH4++AlO2-+2H2O |
15. 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )| A. | Ⅱ表示的是滴定氨水的曲线,当V(HCI)=20 mL时,有:c(Cl-)>c(N${{H}_{4}}^{+}$)>c(H+)>c(OH-) | |
| B. | 当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(N${{H}_{4}}^{+}$)=c(Cl-) | |
| C. | 滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(N${{H}_{4}}^{+}$)-c(NH3•H2O) |
12.放射性同位素钬${\;}_{67}^{166}$Ho的原子核内的中子数与质子数之差是( )
| A. | 166 | B. | 99 | C. | 67 | D. | 32 |
16.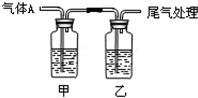 利用如图所示装置进行实验,有关现象和解释均正确的是( )
利用如图所示装置进行实验,有关现象和解释均正确的是( )
 利用如图所示装置进行实验,有关现象和解释均正确的是( )
利用如图所示装置进行实验,有关现象和解释均正确的是( )| 选项 | 足量 气体A | 甲中试剂 | 乙中试剂 | 现象 | 解释 |
| A | CO2 | Na2SiO3 | BaCl2 | 甲浑浊、乙澄清 | 酸性:HCl>H2CO3>H2SiO3 |
| B | Cl2 | 紫色石蕊 | Fe(SCN)2 | 开始均变红 | Cl2溶于水显酸性 |
| C | SO2 | 品红溶液 | KMnO4 | 均褪色 | SO2具有漂白性 |
| D | NH3 | AgNO3 | AlCl3 | 现象相同 | NH3•H2O电离出OH- |
| A. | A | B. | B | C. | C | D. | D |
13.电解NO制备NH4NO3,其工作原理如图所示,下列说法不正确的是( )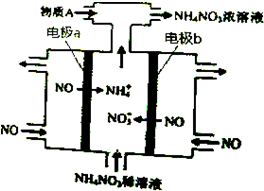

| A. | b极的电极反应为:NO-3e-+2H2O=NO3-+4H+ | |
| B. | 溶液中的H+由电极a处向电极b处迁移 | |
| C. | 电解过程总反应的化学方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3 | |
| D. | 为使电解产物全部转化为NH4NO3,需补充的物质A是NH3 |
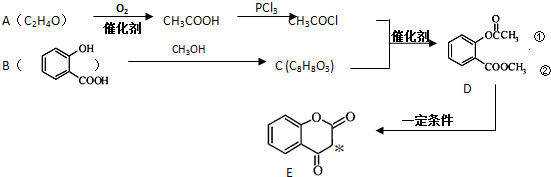
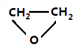 .
.