题目内容
下列关于强、弱电解质的叙述中正确的是( )
| A、强电解质都是离子化合物,弱电解质都是共价化合物 |
| B、强电解质都是可溶性化合物,弱电解质都是难溶性化合物 |
| C、强电解质熔化时都完全电离,弱电解质在水溶液中部分电离 |
| D、强电解质不一定能导电,弱电解质溶液的导电能力不一定比强电解质弱 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.根据物质类别与强弱电解质的关系分析;
B.根据物质溶解性与强弱电解质的关系分析;
C.根据强弱电解质的电离程度分析;
D.溶液的导电能力取决于溶液中自由移动离子的多少.
B.根据物质溶解性与强弱电解质的关系分析;
C.根据强弱电解质的电离程度分析;
D.溶液的导电能力取决于溶液中自由移动离子的多少.
解答:
解:A、HCl等共价化合物也属于强电解质,故A错误;
B、强弱电解质与物质的溶解性没有必然的联系,故B错误;
C、强电解质熔化时不一定电离,如液态氯化氢,在水溶液中完全电离;弱电解质部分电离,溶液中含有电解质分子,故C错误;
D、强电解质不一定能导电,如固态氢氧化钠不导电;溶液的导电能力取决于溶液中自由移动离子的多少,和电解质的强弱无直接关系,故D正确,
故选D.
B、强弱电解质与物质的溶解性没有必然的联系,故B错误;
C、强电解质熔化时不一定电离,如液态氯化氢,在水溶液中完全电离;弱电解质部分电离,溶液中含有电解质分子,故C错误;
D、强电解质不一定能导电,如固态氢氧化钠不导电;溶液的导电能力取决于溶液中自由移动离子的多少,和电解质的强弱无直接关系,故D正确,
故选D.
点评:本题考查强、弱电解质的概念区别及其特性,难度中等.

练习册系列答案
相关题目
下列有机物的命名正确的是( )
A、 3-甲基-2-乙基戊烷 3-甲基-2-乙基戊烷 |
| B、(CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 |
C、 邻甲基苯酚 邻甲基苯酚 |
D、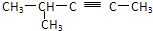 2-甲基-3-戊炔 2-甲基-3-戊炔 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铜溶液中加入铁粉反应:Cu2++Fe=Fe2++Cu |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
四种有机物如下:①?CH2=CH-CH2OH,?②CH3CH2CH2OH,③?CH2=CH-COOH,?④CH2=CH-COOCH3,其中既能发生酯化反应,又能发生加成和氧化反应的是( )
| A、只有? | B、??②③ |
| C、??①③ | D、???①③④ |
旨在遏制全球气候变暖的《京都议定书》2005年2月16日正式生效,受到限制的气体包括人为排出的二氧化碳、甲烷、一氧化二氮、氟化烃、全氟化碳以及六氟化硫六种气体的排放量.下列有关说法正确的是( )
| A、控制温室气体排放,遏制全球变暧趋势是社会可持续发展的保证 |
| B、CH4是目前全球变暧的最主要的温室气体 |
| C、N2O不仅能引起温室效应还与臭氧层破坏、酸雨及化学烟雾有关 |
| D、为减少二氧化碳这种温室气体的排放,不使用含碳能源 |
阿佛加德罗定律能够成立的本质原因是在一定温度和压强下( )
| A、气体体积的大小只随分子数的多少而变化 |
| B、不同气体分子的大小几乎相等 |
| C、不同气体分子间的平均距离几乎相等 |
| D、气体分子间的平均距离与分子本身的大小成正比 |
 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )| A、H2R2的分子中既含有极性共价键,又含有非极性共价键 |
| B、Q、R的简单氢化物分子所含质子数、电子数与Ne分子相同 |
| C、T的氧化物是一种良好的半导体材料 |
| D、Q的氢化物与W的氢化物反应有白烟现象,且生成物中既含有离子键,又含有共价键 |