题目内容
19.向盛有溴化钾溶液的试管中加入少量氯水和CCl4后,充分振荡,可观察到液体分层,其中( )| A. | 上层紫色,下层无色 | B. | 上层近无色,下层橙红色 | ||
| C. | 上层近无色,下层棕黄色 | D. | 上层黄绿色,下层紫红色 |
分析 依据氯气具有强的氧化性,与溴化钾溶于反应生成单质溴,单质溴易溶于有机溶剂而显橙色,CCl4不溶于水,密度大于水分析解答.
解答 解:氯气具有强的氧化性,通入溴化钾溶于发生反应:Cl2+2KBr=2KCl+Br2,反应后得到橙黄色的溴水溶液,倒入CCl4后,CCl4不溶于水,密度大于水,溶液分层,CCl4层在下层,溴在CCl4中的溶解度大于在水中的溶解度,振荡后,溴由被萃取到CCl4层,所以看到的现象是溶液分层,上层为无色的水层,下层为橙色的溶有溴的CCl4层,
故选B.
点评 本题考查了氯气的氧化性和萃取的原理,题目难度不大,熟悉氯气的性质,明确溴在CCl4中溶解度大是解题的关键.

练习册系列答案
相关题目
9.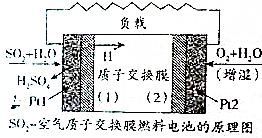 二氧化硫、空气质子交换膜电池将化学能默认变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示,下列说法错误的是( )
二氧化硫、空气质子交换膜电池将化学能默认变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示,下列说法错误的是( )
 二氧化硫、空气质子交换膜电池将化学能默认变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示,下列说法错误的是( )
二氧化硫、空气质子交换膜电池将化学能默认变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示,下列说法错误的是( )| A. | Pt1电极附近发生的反应为SO2+2H2O-2e-═SO42-+4H+ | |
| B. | Pt2电极附近发生的反应为O2+4e-═2O2- | |
| C. | 该电池放电时电子从Pt1电极经过外电路流到Pt2电极 | |
| D. | 相同条件下,放电过程中消耗的SO2和O2的体积之比为2:1 |
10.下列有关金属的说法中正确的是( )
| A. | 铝在空气中能生成一层致密的氧化物保护膜 | |
| B. | 铜的化学性质不活泼,在潮湿的空气中也不生锈 | |
| C. | 钛具有耐腐蚀性,可用来制造海轮的外壳 | |
| D. | 镀锌的“白铁皮”不易生锈,说明锌没有铁活泼 |
7.如图所示是“能源相关图”,下列四组能源选项中全部符合图中阴影部分能源的是( )


| A. | 煤炭、石油、沼气 | B. | 风能、太阳能、沼气 | ||
| C. | 地热能、海洋能、核能 | D. | 生物质能、天然气、水能 |
14.下列说法不正确的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | NaHCO3的热稳定性大于Na2CO3 | ||
| C. | 水可与金属钠反应放出氢气 | D. | 金属钠保存在煤油中 |
4.下列物质中,属于强电解质的是( )
| A. | SO3 | B. | CH3COOH | C. | NH3•H2O | D. | Ba(OH)2 |
11.下列溶液中有关物质的量浓度关系或计算正确的是( )
| A. | pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有:C(NaOH)<C(CH3COONa)<C(NaHCO3) | |
| B. | 25℃时,0.1 mol•L-1 Na2CO3溶液中水电离出来的C(OH-)大于0.1 mol•L-1 NaOH溶液中水电离出来的C(OH-) | |
| C. | 常温下物质的量浓度相等的①(NH4)2Fe(SO4)2②(NH4 )2CO3;③(NH4)2SO4三种溶液中c(NH4+):①>②>③ | |
| D. | 室温下,0.1 mol•L-1 NaHA溶液的pH=4,则C(HA-)>C(H+)>C(H2A)>C(A2ˉ) |
8.乙炔和苯的混合物13g完全燃烧后生成CO2和H2O,消耗氧气的质量为( )
| A. | 40g | B. | 20g | C. | 32g | D. | 无法计算 |
9.下列各物质中,属于电解质的是( )
| A. | 盐酸 | B. | 硫酸钡 | C. | 蔗糖 | D. | 浓氨水 |