题目内容
某结晶水合物化学式X?nH2O,其相对分子质量为M,在25℃时,A g该结晶水合物溶于B g水中即可达到饱和,形成密度为D g/cm3的饱和饱和溶液V mL,下列表达式中不正确的是( )
分析:A、计算Ag该结晶水合物中X的质量,利用m=ρV计算溶液的质量,再利用质量分数的定义计算.
B、计算Ag该结晶水合物中X的质量,形成溶液中水的质量为Bg+Ag该结晶水合物的中水的质量,根据溶解度定义计算.
C、溶液质量为(A+B)g,溶液VmL,质量除以溶液体积为溶液密度.
D、计算Ag该结晶水合物的物质的量,即为X的物质的量,溶液溶液VmL,利用c=
计算.
B、计算Ag该结晶水合物中X的质量,形成溶液中水的质量为Bg+Ag该结晶水合物的中水的质量,根据溶解度定义计算.
C、溶液质量为(A+B)g,溶液VmL,质量除以溶液体积为溶液密度.
D、计算Ag该结晶水合物的物质的量,即为X的物质的量,溶液溶液VmL,利用c=
| n |
| V |
解答:解:A、Ag该结晶水合物X?nH2O中X的质量为Ag×
,密度为Dg/cm3,溶液VmL,则溶液的质量为DVg,所以溶液的质量分数为
×100%=
%,故A正确;
B、Ag该结晶水合物X?nH2O中X的质量为Ag×
,溶剂水的质量为Bg+Ag×
,令该温度下,溶解度为Sg,则
100g:Sg=(Bg+Ag×
):Ag×
,解得S=
,故B正确;
C、溶液质量为(A+B)g,溶液VmL,所以溶液密度为
g/ml,故C正确;
D、Ag该结晶水合物X?nH2O的物质的量为
mol,所以X的物质的量为
mol,溶液溶液VmL,物质的量浓度c=
=
mol/L,故D错误.
故选:D.
| M-18n |
| M |
| ||
| DV |
| 100A(M-18n) |
| MVD |
B、Ag该结晶水合物X?nH2O中X的质量为Ag×
| M-18n |
| M |
| 18n |
| M |
100g:Sg=(Bg+Ag×
| 18n |
| M |
| M-18n |
| M |
| 100A(M-18n) |
| BM+18An |
C、溶液质量为(A+B)g,溶液VmL,所以溶液密度为
| A+B |
| V |
D、Ag该结晶水合物X?nH2O的物质的量为
| A |
| M |
| A |
| M |
| ||
| V×10-3L |
| 1000A |
| MV |
故选:D.
点评:考查溶解度、质量分数、物质的量浓度的计算与相互关系,难度中等,注意公式的灵活运用.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
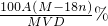
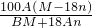 克
克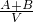 g/cm3
g/cm3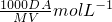
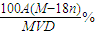
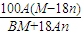 克
克 g/cm3
g/cm3