��Ŀ����
������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�������������Ҫ�������£�
��1����N2��H2Ϊԭ�Ϻϳɰ�������ӦN2��g��+3H2��g��?2NH3��g����H��0
�����д�ʩ�������H2��ת�����ǣ���ѡ����ţ� ��
a��ѡ���ʵ��Ĵ��� b������ѹǿ c����ʱ�������ɵ�NH3 d�������¶�
��һ���¶��£����ܱ������г���1molN2��3molH2������Ӧ���������ݻ��㶨���ﵽƽ��״̬ʱ�������ڵ�ѹǿ��ԭ����
����N2��ת����a1= ��
������ѹǿ�㶨���ﵽƽ��״̬ʱ��N2��ת����Ϊa2����a2 a1�����������������=������
��2������������Ϊ��Ҫԭ�������ᣮ
��NH3����������������NO�ķ�Ӧ�Ļ�ѧ����ʽ�� ��
�����ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O2��g��?2NO2��g����H��0
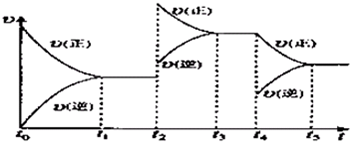
�÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��ͼ��ʾ����t2��t4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ� ��
a����t1��t2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
b����t2ʱ����ȡ�Ĵ�ʩһ���������¶�
c����t3��t4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
d����t0��t5ʱ��������NO2�����������t3ʱֵ�����
�����ݻ���ͬ���¶ȷֱ�ΪT1��T2�������ܱ������зֱ�������NO2������Ӧ��
2NO2 ��g��?N2O4��g����H��0�����º����·�Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ����ֱ�Ϊa1��a2����֪T1��T2����a1 a2
A������ B��С�� C������ D�����϶��п���
��3�����᳧��������2�ַ�������β����
�ٴ���ԭ������������ʱ��H2��NO2��ԭΪN2��
��֪��2H2��g��+O2��g��=2H2O��g����H=-483.5kJ/mol
N2��g��+2O2��g��=2NO2��g����H=+133kJ/mol
��H2��ԭNO2����ˮ������Ӧ���Ȼ�ѧ����ʽ�� ��
�ڼ�Һ���շ�����Na2CO3��Һ����NO2����CO2��
��ÿ9.2gNO2��Na2CO3��Һ��Ӧʱת�Ƶ�����Ϊ0.1mol����Ӧ�����ӷ���ʽ�� ��

��1����N2��H2Ϊԭ�Ϻϳɰ�������ӦN2��g��+3H2��g��?2NH3��g����H��0
�����д�ʩ�������H2��ת�����ǣ���ѡ����ţ�
a��ѡ���ʵ��Ĵ��� b������ѹǿ c����ʱ�������ɵ�NH3 d�������¶�
��һ���¶��£����ܱ������г���1molN2��3molH2������Ӧ���������ݻ��㶨���ﵽƽ��״̬ʱ�������ڵ�ѹǿ��ԭ����
| 15 | 16 |
������ѹǿ�㶨���ﵽƽ��״̬ʱ��N2��ת����Ϊa2����a2
��2������������Ϊ��Ҫԭ�������ᣮ
��NH3����������������NO�ķ�Ӧ�Ļ�ѧ����ʽ��
�����ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O2��g��?2NO2��g����H��0
�÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��ͼ��ʾ����t2��t4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ�
a����t1��t2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
b����t2ʱ����ȡ�Ĵ�ʩһ���������¶�
c����t3��t4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
d����t0��t5ʱ��������NO2�����������t3ʱֵ�����
�����ݻ���ͬ���¶ȷֱ�ΪT1��T2�������ܱ������зֱ�������NO2������Ӧ��
2NO2 ��g��?N2O4��g����H��0�����º����·�Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ����ֱ�Ϊa1��a2����֪T1��T2����a1
A������ B��С�� C������ D�����϶��п���
��3�����᳧��������2�ַ�������β����
�ٴ���ԭ������������ʱ��H2��NO2��ԭΪN2��
��֪��2H2��g��+O2��g��=2H2O��g����H=-483.5kJ/mol
N2��g��+2O2��g��=2NO2��g����H=+133kJ/mol
��H2��ԭNO2����ˮ������Ӧ���Ȼ�ѧ����ʽ��
�ڼ�Һ���շ�����Na2CO3��Һ����NO2����CO2��
��ÿ9.2gNO2��Na2CO3��Һ��Ӧʱת�Ƶ�����Ϊ0.1mol����Ӧ�����ӷ���ʽ��
��������1�������H2��ת���ʣ�Ӧʹƽ��������Ӧ�ƶ����ݴ˽�����������ƽ����Ӱ��������
������ѹǿ֮�ȵ������ʵ���֮�ȼ���ƽ��ʱ��Ӧ�������ܵ����ʵ����������ò���������μӷ�Ӧ�ĵ��������ʵ��������ö������N2��ת���ʣ�
����Ӧ�����������С�ķ�Ӧ������ѹǿ�㶨���൱���ں��ݵ�����������ѹǿ��ƽ��������Ӧ���У�������ת��������
��2���ٰ�������������������һ��������ˮ����ƽ��д����ʽ��
��a���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣻
b������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ���
c�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣻
d����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ�
�������¶�ƽ�����淴Ӧ���У�ƽ��ʱ���������ĺ��������¶�Խ�߷�Ӧ����Խ�죬����ƽ���ʱ��Խ�̣��ݴ�������������������ʱ���ϵ��ͼ���ݴ��жϣ�
��3���ٸ��ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ӧ��Ҳ������Ӧ��ϵ����������Ӧ�����㣻
�ڸ���n=
����NO2�����ʵ�������Ӧ��ֻ��NO2��NԪ�ػ��ϼ۷����仯�������绯��Ӧ��������NO3-������ע���������������NO3-�����ʵ������ٸ��ݵ���ת���غ����NԪ���ڻ�ԭ�����еĻ��ϼۣ��жϻ�ԭ����ݴ���д��
������ѹǿ֮�ȵ������ʵ���֮�ȼ���ƽ��ʱ��Ӧ�������ܵ����ʵ����������ò���������μӷ�Ӧ�ĵ��������ʵ��������ö������N2��ת���ʣ�
����Ӧ�����������С�ķ�Ӧ������ѹǿ�㶨���൱���ں��ݵ�����������ѹǿ��ƽ��������Ӧ���У�������ת��������
��2���ٰ�������������������һ��������ˮ����ƽ��д����ʽ��
��a���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣻
b������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ���
c�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣻
d����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ�
�������¶�ƽ�����淴Ӧ���У�ƽ��ʱ���������ĺ��������¶�Խ�߷�Ӧ����Խ�죬����ƽ���ʱ��Խ�̣��ݴ�������������������ʱ���ϵ��ͼ���ݴ��жϣ�
��3���ٸ��ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ӧ��Ҳ������Ӧ��ϵ����������Ӧ�����㣻
�ڸ���n=
| m |
| M |
����⣺��1���١�a��ѡ���ʵ��Ĵ������ӿ췴Ӧ���ʣ���Ӱ��ƽ���ƶ���H2��ת���ʲ��䣬��a����
b������ѹǿ��ƽ��������Ӧ�ƶ���H2��ת��������b��ȷ��
c����ʱ�������ɵ�NH3��������Ũ�Ƚ��ͣ�ƽ��������Ӧ�ƶ���H2��ת��������c��ȷ��
d�������¶ȣ�ƽ�����淴Ӧ�ƶ���H2��ת���ʽ��ͣ���d����
�ʴ�Ϊ��bc��
��ѹǿ֮�ȵ������ʵ���֮�ȣ��ﵽƽ��״̬ʱ�������ڵ�ѹǿ��ԭ����
������ٵ����ʵ���Ϊ��1+3��mol��(1-
)=
mol����
N2��g��+3H2��g��?2NH3��g�� ���ʵ������١�n
1 2
n��N2��
mol
��n��N2��=
=
mol�����Ե�����ת����=
��100%=12.5%��
����Ӧ�����������С�ķ�Ӧ������ѹǿ�㶨���൱���ں��ݵ�����������ѹǿ��ƽ��������Ӧ���У�������ת������������a2��a1��
�ʴ�Ϊ��12.5%������
��2���ٰ����Ĵ�������Ӧ����ʽΪ��4NH3+5O2
4NO+6H2O���ʴ�Ϊ��4NH3+5O2
4NO+6H2O��
��a���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣬��a��ȷ��
b������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ�����t2ʱ�����������ʶ�����������Ӧ����������࣬ƽ��������Ӧ�ƶ����÷�Ӧ����Ӧ�����������С�ķ�Ӧ������ѹǿƽ��������Ӧ���У���t2ʱΪ����ѹǿ����b����
c�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬����c����
d����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ�����d��ȷ��
��ѡad��
�������¶�ƽ�����淴Ӧ���У�ƽ��ʱ���������ĺ��������¶�Խ�߷�Ӧ����Խ�죬����ƽ���ʱ��Խ�̣��ݴ�������������������ʱ���ϵ��ͼΪ ����ͼ��֪��t1ʱ��a1=a2��t1ʱ��֮ǰa1��a2��t1ʱ��֮��a1��a2���ʴ�Ϊ��D��
����ͼ��֪��t1ʱ��a1=a2��t1ʱ��֮ǰa1��a2��t1ʱ��֮��a1��a2���ʴ�Ϊ��D��
��3������֪����2H2��g��+O2��g��=2H2O��g����H=-483.5kJ/mol
��N2��g��+2O2��g��=2NO2��g����H=+133kJ/mol
�ɸ�˹���ɿ�֪�����2-���4H2��g��+2NO2��g��=N2��g��+4H2O��g����
�ʡ�H=2����-483.5kJ/mol��-133kJ/mol=-1100kJ/mol��
���Ȼ�ѧ����ʽΪ��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100kJ/mol��
�ʴ�Ϊ��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100kJ/mol��
��9.2gNO2�����ʵ���=
mol=0.2mol����Ӧ��ֻ��NO2��NԪ�ػ��ϼ۷����仯�������绯��Ӧ��������NO3-��
0.2mol��������ת�Ƶ��ӵ����ʵ�����0.1mol�������ɵ�NO3-�����ʵ���Ϊ
=0.1mol���ʱ���ԭ�ĵ�ԭ�����ʵ���Ϊ0.2mol-0.1mol=0.1mol����NԪ���ڻ�ԭ�����еĻ��ϼ�Ϊx�ۣ���0.1mol����4-x��=0.1mol�����x=+3���ʻ�ԭ����ΪNO2-�������ɵ�NO3-��NO2-���ʵ���֮��Ϊ1��1��ͬʱ��Ӧ����CO2���ʶ���������̼������Һ��Ӧ�����ӷ�Ӧ����ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2���ʴ�Ϊ��2NO2+CO32-=NO3-+NO2-+CO2��
b������ѹǿ��ƽ��������Ӧ�ƶ���H2��ת��������b��ȷ��
c����ʱ�������ɵ�NH3��������Ũ�Ƚ��ͣ�ƽ��������Ӧ�ƶ���H2��ת��������c��ȷ��
d�������¶ȣ�ƽ�����淴Ӧ�ƶ���H2��ת���ʽ��ͣ���d����
�ʴ�Ϊ��bc��
��ѹǿ֮�ȵ������ʵ���֮�ȣ��ﵽƽ��״̬ʱ�������ڵ�ѹǿ��ԭ����
| 15 |
| 16 |
| 15 |
| 16 |
| 1 |
| 4 |
N2��g��+3H2��g��?2NH3��g�� ���ʵ������١�n
1 2
n��N2��
| 1 |
| 4 |
��n��N2��=
1��
| ||
| 2 |
| 1 |
| 8 |
| ||
| 1mol |
����Ӧ�����������С�ķ�Ӧ������ѹǿ�㶨���൱���ں��ݵ�����������ѹǿ��ƽ��������Ӧ���У�������ת������������a2��a1��
�ʴ�Ϊ��12.5%������
��2���ٰ����Ĵ�������Ӧ����ʽΪ��4NH3+5O2
| ���� |
| �� |
| ���� |
| �� |
��a���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣬��a��ȷ��
b������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ�����t2ʱ�����������ʶ�����������Ӧ����������࣬ƽ��������Ӧ�ƶ����÷�Ӧ����Ӧ�����������С�ķ�Ӧ������ѹǿƽ��������Ӧ���У���t2ʱΪ����ѹǿ����b����
c�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬����c����
d����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ�����d��ȷ��
��ѡad��
�������¶�ƽ�����淴Ӧ���У�ƽ��ʱ���������ĺ��������¶�Խ�߷�Ӧ����Խ�죬����ƽ���ʱ��Խ�̣��ݴ�������������������ʱ���ϵ��ͼΪ
 ����ͼ��֪��t1ʱ��a1=a2��t1ʱ��֮ǰa1��a2��t1ʱ��֮��a1��a2���ʴ�Ϊ��D��
����ͼ��֪��t1ʱ��a1=a2��t1ʱ��֮ǰa1��a2��t1ʱ��֮��a1��a2���ʴ�Ϊ��D����3������֪����2H2��g��+O2��g��=2H2O��g����H=-483.5kJ/mol
��N2��g��+2O2��g��=2NO2��g����H=+133kJ/mol
�ɸ�˹���ɿ�֪�����2-���4H2��g��+2NO2��g��=N2��g��+4H2O��g����
�ʡ�H=2����-483.5kJ/mol��-133kJ/mol=-1100kJ/mol��
���Ȼ�ѧ����ʽΪ��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100kJ/mol��
�ʴ�Ϊ��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100kJ/mol��
��9.2gNO2�����ʵ���=
| 9.2 |
| 46 |
0.2mol��������ת�Ƶ��ӵ����ʵ�����0.1mol�������ɵ�NO3-�����ʵ���Ϊ
| 0.1mol |
| (5-4) |
���������⿼�黯ѧƽ����йؼ��㡢��ѧƽ���Ӱ��������ƽ��ͼ���Ȼ�ѧ����ʽ��д��������ԭ��Ӧ�ȣ���Ŀ�ۺ��Խϴ��ѶȽϴ�ע�⣨2���Т����ú���-ʱ���ͼ�������⣬�����Ƿ�ƽ�⣬���ݸ�����жϣ�

��ϰ��ϵ�д�
 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
�����Ŀ
 ��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��
��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g�� FeO��s��+CO��g������H��0
FeO��s��+CO��g������H��0