题目内容
某化学兴趣小组为了探究铬和铁的活泼性,设计如图所示装置,下列推断合理的是( )


| A、若铬比铁活泼,则电子经外电路由铁电极流向铬电极 |
| B、若铬比铁活泼,则铁电极反应式为2H++2e-=H2↑ |
| C、若铁比铬活泼,则溶液中H+向铁电极迁移 |
| D、若铁电极附近溶液pH增大,则铁比铬活泼 |
考点:原电池和电解池的工作原理
专题:
分析:若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,电子经外电路由铬电极流向铁电极;若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子在铬上得电子发生还原反应,电子经外电路由铁电极流向铬电极.
解答:
解:A.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,电子经外电路由铬电极流向铁电极,故A错误;
B.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,反应式为2H++2e-=H2↑,故B正确;
C.若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子向正极铬移动,故C错误;
D.若铁电极附近溶液pH增大,则发生2H++2e-=H2↑,所以铁为正极,则铬比铁活泼,故D错误.
故选:B.
B.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,反应式为2H++2e-=H2↑,故B正确;
C.若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子向正极铬移动,故C错误;
D.若铁电极附近溶液pH增大,则发生2H++2e-=H2↑,所以铁为正极,则铬比铁活泼,故D错误.
故选:B.
点评:本题主要考查了原电池的原理,掌握基础是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 国庆节期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )
国庆节期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )| A、其分子式为C15H21O4 |
| B、该有机物能发生取代、加成和水解反应 |
| C、1mol的该有机物与足量的钠反应产生1molH2 |
| D、该有机物不能使酸性KMnO4溶液褪色 |
香兰素是重要的香料之一,它可由丁香酚经多步反应合成,有关上述两种化合物的说法正确的是( )
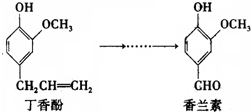

| A、香兰素分子中至少有12个原子共平面 |
| B、丁香酚不能与三氯化铁溶液发生显色反应 |
| C、1mol香兰素最多能与3mol氢气发生加成反应 |
| D、常温下1mol丁香酚只能与1molBr2反应 |
下列各组离子在溶液中能大量共存的是( )
| A、Na+、OH-、S2O32-、Cl- |
| B、Fe2+、K+、[Fe(CN)6]3-、NO3- |
| C、H+、C2O42-、MnO4-、SO42- |
| D、Na+、Ca2+、AlO2-、HCO3- |
下列不能通过化合反应得到的是( )
| A、氢氧化铁 | B、氢氧化铝 |
| C、盐酸 | D、碳酸氢钠 |
下列各项比较中前者高于(或大于或强于)后者的是( )
| A、CH4和SiH4的熔点 |
| B、I2在H2O中的溶解能力和I2在CCl4中的溶解能力 |
| C、H2SO3和H2SO4的酸性 |
D、对羟基苯甲醛( )和邻羟基苯甲醛( )和邻羟基苯甲醛( )的沸点 )的沸点 |
设NA代表阿伏加德罗常数,下列说法中正确的是( )
| A、7.1gCl2与足量的铁反应转移电子数目为0.3NA |
| B、17g甲基(-14CH3)中含有的质子数为8NA |
| C、48gO2和O3的混合物含有的原子数为3NA |
| D、100mL0.5 mol/L 的乙酸溶液中分子总数小于0.05NA |
下列原子团中,属于烃基的是( )
| A、-CH3 |
| B、-OH |
| C、-COOH |
| D、OH- |