题目内容
6.关于有机物性质或应用的叙述正确的是( )| A. | 乙烯和苯都能使溴水褪色,褪色的原理相同 | |
| B. | 由甲苯硝化制三硝基甲苯(TNT)和由甲苯氧化制苯甲酸属于同一种反应类型 | |
| C. | 煤油可由石油分馏获得,可用作燃料和保存少量金属钠 | |
| D. | 除去C2H2中的杂质H2S,可依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
分析 A.乙烯与溴水发生加成反应,苯与溴水发生萃取;
B.由甲苯硝化制三硝基甲苯(TNT),苯环上H被取代,而由甲苯氧化制苯甲酸,O原子增多;
C.石油为烃的混合物,分离出煤油为混合物,且煤油与Na不反应,Na的密度比煤油密度大;
D.C2H2、H2S均能被高锰酸钾氧化.
解答 解:A.乙烯与溴水发生加成反应,苯与溴水发生萃取,分别发生化学变化、物理变化,褪色原理不同,故A错误;
B.由甲苯硝化制三硝基甲苯(TNT),苯环上H被取代,而由甲苯氧化制苯甲酸,O原子增多,分别为取代反应、氧化反应,故B错误;
C.石油为烃的混合物,分离出煤油为混合物,且煤油与Na不反应,Na的密度比煤油密度大,则煤油可用作燃料和保存少量金属钠,故C正确;
D.C2H2、H2S均能被高锰酸钾氧化,则不能除杂,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
16.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 酸雨的形成CO2+H2O═H2CO3化合反应 | |
| B. | 干粉灭火器的反应原理6NaHCO3+2Al2(SO4)3═3Na2SO4+6CO2↑+Al(OH)3↓复分解反应 | |
| C. | 用稀硫酸洗去附着在试管壁上的铜Cu+H2SO4═CuSO4+H2↑ 置换反应 | |
| D. | 误服用氯化钡后用硫酸镁解毒BaCl2+MgSO4═MgCl2+BaSO4↓ 复分解反应 |
17.用NA表示阿伏加德罗常数的值,卞列叙述正确的是( )
| A. | 含有NA个原子的氢气在标准状况下的体积约为22.4L | |
| B. | 25℃,1.01×105Pa,64gS02中含有的原子数为3NA | |
| C. | 40gNaOH溶解在1L水中,则其100 mL溶液中含Na+数为0.1NA | |
| D. | 标准状况下,11.2 LH20含有的分子数为0.5NA |
14.下列实验操作中错误的是( )
| A. | 用四氯化碳萃取碘水中的碘的实验,分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 蒸发结晶时剩余少量液体停止加热 | |
| D. | 称量时,称量物放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
1.高锰酸钾(KMnO4)是一种强氧化剂,在化学实验中被大量使用,下列关于它的性质和用途的叙述正确的是( )
| A. | 为了增强其氧化性,在配制时加入一定浓度的盐酸 | |
| B. | 该物质在反应中可以被还原,也可以被氧化 | |
| C. | 可用酸化的KMnO4溶液除去甲烷中的乙烯 | |
| D. | KMnO4中Mn元素为其最高价+7,故含有最高价元素的化合物,均有强氧化性,如浓硫酸、浓硝酸 |
11.下列离子方程式正确的是( )
| A. | 铁粉与稀硫酸反应:2Fe+6H+═2Fe3++3H2 | |
| B. | 碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-═CO2↑+H2O | |
| C. | 氯化钙溶液与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 铜片插入硝酸银溶液中Cu+2Ag+═Cu2++2Ag |
15.下列行为中符合安全要求的是( )
| A. | 进入煤矿矿井时,用火把照明 | |
| B. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| C. | 实验时,蒸发结晶时,当有大量晶体析出时再用玻璃棒搅拌 | |
| D. | 装运乙醇的包装箱上应贴上易燃液体的危险品标志图标 |
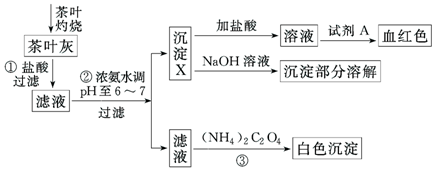
16.某化学兴趣小组设计以下实验步骤与操作来定性检验茶叶中含有的少量钙、铁、铝三种元素.
已知Ca2+、Al2+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
(1)步骤①中加入盐酸的作用是使茶叶中的钙、铁、铝元素转化为离子.
(2)步骤②中调节pH至6~7的目的是使Fe3+、Al3+转化为沉淀.
(3)沉淀X所含主要物质的化学式为Al(OH)3、Fe(OH)3 .
(4)写出沉淀X与NaOH溶液反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O;写出步骤③中发生反应的离子方程式:Ca2++C2O42-=CaC2O4↓.
(5)试剂A为硫氰化钾溶液.

已知Ca2+、Al2+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
| Ca(OH)2 | Al(OH)3 | Fe(OH)3 | |
| pH | ≥13 | ≥5.2 | ≥4.1 |
(2)步骤②中调节pH至6~7的目的是使Fe3+、Al3+转化为沉淀.
(3)沉淀X所含主要物质的化学式为Al(OH)3、Fe(OH)3 .
(4)写出沉淀X与NaOH溶液反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O;写出步骤③中发生反应的离子方程式:Ca2++C2O42-=CaC2O4↓.
(5)试剂A为硫氰化钾溶液.