题目内容
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)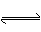 2C(g),若经 2 s(秒)后测得C的浓度为0.6 mol·L-1 ,现有下列几种说法,其中正确的是
2C(g),若经 2 s(秒)后测得C的浓度为0.6 mol·L-1 ,现有下列几种说法,其中正确的是
A.用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
B.用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1
C.2 s 时物质 A的转化率为70%
D.2 s 时物质 B的浓度为 0.7 mol·L-1
AD
【解析】
试题分析:根据三段式2A(g)+B(g) 2C(g)
2C(g)
开始浓度(mol/L) 2 1 0
变化浓度(mol/L) 0.6 0.3 0.6
平衡浓度(mol/L) 1.4 0.7 0.6
A、用物质 A 表示的反应的平均速率为 0.6/2=0.3 mol·L-1·s-1,正确;B、用物质 B 表示的反应的平均速率为0.3/2=0.15 mol·L-1·s-1,错误;C、2 s 时物质 A的转化率为(0.6/2)×100%=30% ,错误;D、2 s 时物质 B的浓度为 0.7 mol·L-1,正确;选AD。
考点:考查化学反应速率的计算。

 名校课堂系列答案
名校课堂系列答案(10分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |

(1)已知升高温度,NO2的浓度减小,则该反应是 热反应。
(2)下图中表示NO2的变化的曲线是 用O2表示从0~2 s内该反应的平均速率v =
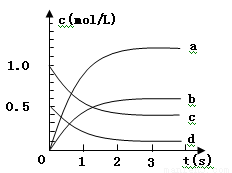
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
 CH3COCH2COH(CH3)2(aq);取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率
CH3COCH2COH(CH3)2(aq);取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率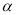 随时间变化的关系曲线(
随时间变化的关系曲线(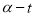 )如图所示。
)如图所示。
 CO (g)+H2O(g) △H>0,达到平衡后,为提高该反应的速率和CO2的转化率,采取的正确措施是
CO (g)+H2O(g) △H>0,达到平衡后,为提高该反应的速率和CO2的转化率,采取的正确措施是