题目内容
17.利用l00mL lmol/L稀硫酸与足量的锌粒反应制取氢气时,下列措施不能加快反应速率的是( )| A. | 滴入少量硫酸铜溶液 | B. | 加入适量2mol/L稀硫酸 | ||
| C. | 适当加热 | D. | 改用200mL lmol/L稀硫酸 |
分析 加热、增大浓度、增大接触面积、构成原电池,均可加快反应速率,以此来解答.
解答 解:A.锌置换出铜,形成铜锌原电池反应,反应速率增大,故A不选;
B.改用2mol/L的硫酸,增大浓度,加快反应速率,故B不选;
C.适当升高温度,增大活化分子百分数,反应速率增大,故C不选;
D.改用200mL lmol/L稀硫酸,浓度不变,则反应速率不变,故D选.
故选D.
点评 本题考查化学反应速率的影响因素,为高考高频考点,侧重于学生的分析能力和基本理论知识的综合运用的考查,难度不大,注意相关基础知识的积累,把握影响化学反应速率的因素.

练习册系列答案
相关题目
8.下列分散系中.分散质粒+直径最小的是( )
| A. | KC1 溶液 | B. | Fe (OH)3胶体 | C. | 牛奶 | D. | 石灰乳 |
12.某烃和溴水反应的产物为2,2,3,3-四溴丁烷,则该烃同分异构体为( )
| A. | 1-丁烯 | B. | 1-丁炔 | C. | 2-丁炔 | D. | 2-丁烯 |
2.丙烯酸(CH2=CH-COOH)的性质可能有( )
①加聚反应②酯化反应③中和反应④氧化反应⑤水解反应.
①加聚反应②酯化反应③中和反应④氧化反应⑤水解反应.
| A. | 只有①③ | B. | 只有②③④ | C. | 只有①④ | D. | 全部 |
6.常温下,分别将四块形状相同,质量均为7g的铁块同时投入下列四种溶液中,铁块首先溶解完的是( )
| A. | 20.0 mL 18 mol•L-1 H2SO4溶液 | B. | 250.0 mL 2 mol•L-1 HCl溶液 | ||
| C. | 150.0 mL 2 mol•L-1 H2SO4溶液 | D. | 500.0 mL 3 mol•L-1 HCl溶液 |
7.碳酸锶( SrCO3)可、作磁、材料、电子元件和焰火材料等.以天青石(主要成分为SrSO4,含有少量BaCO3.FeO.Fe2O3、Al2O3、SiO2等)为原料制备SrCO3的工艺流程如图1:

已知:
回答下列问题:
(I)写出一条能加快“浸取转化”反应速率的措施:升高温度增大纯碱浓度;滤液1的主要成分为Na2SO4(填化学式).
(2)加入HC1、HNO3混酸溶解后,所得溶液中阳离子共有5种;滤渣1的主要成分为SiO2(填化学式).
(3)“除钡”过程中硫酸过多会导致锶元素的损失.若除钡后所得溶液(M)中c(Ba2+)=1.0×10-5mol•L-1,要使锶元素不损失,则M中c(Sr2+)应不超过0.029mol•L-1(计算结果保留2位有效数字).
(4)“沉锶”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3+H2O+CO2↑.“沉锶”过程中锶的转化率随温度变化如图2所示,60℃之前,锶的转化率随温度升高而变大的主要原因是升温有利于二氧化碳逸出有利于SrCO3生成.
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;高温\;}}{\;}$2Sr+3SrO•Al2O3.

已知:
| SrSO4 | BaSO4 | SrCO3 | |
| Ksp | 3.2×10-7 | 1.1×10-10 | 1.6×10-10 |
(I)写出一条能加快“浸取转化”反应速率的措施:升高温度增大纯碱浓度;滤液1的主要成分为Na2SO4(填化学式).
(2)加入HC1、HNO3混酸溶解后,所得溶液中阳离子共有5种;滤渣1的主要成分为SiO2(填化学式).
(3)“除钡”过程中硫酸过多会导致锶元素的损失.若除钡后所得溶液(M)中c(Ba2+)=1.0×10-5mol•L-1,要使锶元素不损失,则M中c(Sr2+)应不超过0.029mol•L-1(计算结果保留2位有效数字).
(4)“沉锶”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3+H2O+CO2↑.“沉锶”过程中锶的转化率随温度变化如图2所示,60℃之前,锶的转化率随温度升高而变大的主要原因是升温有利于二氧化碳逸出有利于SrCO3生成.
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;高温\;}}{\;}$2Sr+3SrO•Al2O3.





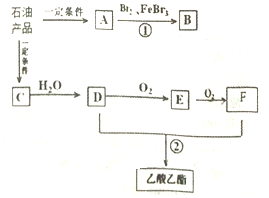 石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去).
石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去). ,反应类型为取代反应;
,反应类型为取代反应;