题目内容
9.能证明乙醇分子中有一个羟基的事实是( )| A. | 乙醇完全燃烧生成CO2和H2O | |
| B. | 0.1mol乙醇与足量钠反应生成0.05molH2 | |
| C. | 乙醇能与水以任意比互溶 | |
| D. | 乙醇能发生氧化反应 |
分析 乙醇中羟基的数目与其燃烧产物、水溶性以及乙醇能发生氧化反应无关,根据乙醇与生成的氢气的物质的量之间的关系可以确定分子中有羟基的数目.
解答 解:A、乙醇燃烧生成二氧化碳和水,只能说明其含碳元素和氢元素,不能说明其含有的羟基的个数,故A错误;
B、乙醇与生成的氢气的物质的量之比为0.1:0.05=2:1,说明乙醇分子中有一个活泼的氢原子可被金属钠取代(置换),即乙醇分子中有一个羟基,故B正确;
C、乙醇能和水以任意比互溶,是由于乙醇和水分子之间能形成氢键,不能说明乙醇中含几个羟基,故C错误;
D、乙醇的氧化分为燃烧和催化氧化,乙醇的燃烧与其中含几个羟基无关,而乙醇能发生催化氧化反应,只能说明乙醇中羟基所在的碳原子上有氢原子,不能说明其结构中的羟基的个数,故D错误.
故选B.
点评 本题考查学生乙醇中羟基的性质,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
20.下列说法错误的是( )
| A. | 钠在空气中燃烧最后所得产物为Na2O2 | |
| B. | 镁因在空气中形成了一层致密的氧化膜,保护了里面的镁,故镁不需要进行特殊保护 | |
| C. | 铝制品在生活中非常普遍,这是因为铝不活泼 | |
| D. | 铁在潮湿的空气中因为生成的氧化膜很疏松不能保护内层金属,故铁制品往往需涂保护层 |
17.下列叙述正确的是( )
| A. | 将钠放入硫酸铜溶液中可置换出铜 | |
| B. | 铜丝在氯气中燃烧,产生蓝色的烟 | |
| C. | 向氯化铁溶液中滴入KOH溶液,可产生红褐色胶体 | |
| D. | 氢气在氯气中燃烧,火焰呈苍白色 |
14.人体血液的pH保持在7.35~7.45,适量的CO2可以维持这个pH变化范围,可用下面的化学方程式表示:H2O+CO2???H2CO3???H++HCO3-,又知人体呼出的气体中CO2的体积分数约为5%,下列说法正确的是( )
| A. | 太快而且太深的呼吸可导致碱中毒 | |
| B. | 太快而且太深的呼吸可导致酸中毒 | |
| C. | 太浅的呼吸可导致碱中毒 | |
| D. | 太浅的呼吸不会导致酸中毒或碱中毒 |
1.C、H、O三种元素组成的T、X在一定条件下可以发生如下转化: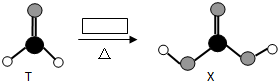
X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )

X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )
| A. | O2 | B. | NaOH溶液 | C. | 稀硫酸 | D. | Na2SO3溶液 |
18.常温下,0.1mol/L的氯化铵溶液中,下列描述及关系不正确的是( )
| A. | 溶液呈酸性 | |
| B. | c(NH3•H2O)+c(NH4+)=0.1mol/L | |
| C. | c(NH4+)+c(H+)=c(OH-)+c(Cl-) | |
| D. | 氯化铵的加入可抑制水的电离,使Kw=1.0×10-14 |
19.对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0 的化学反应,下列叙述错误的是( )
| A. |  反应过程中能量关系可用如图表示 | |
| B. | 若将该反应设计成原电池则锌为负极 | |
| C. | △H的值与反应方程式的化学计量数有关 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,转移电子数为2NA |
 ,食醋中的有机物结构式
,食醋中的有机物结构式 ,糖尿病患者尿液中含的糖类结构简式CH2(OH)CH(OH)CH(OH)CH(OH) CH(OH)CHO.
,糖尿病患者尿液中含的糖类结构简式CH2(OH)CH(OH)CH(OH)CH(OH) CH(OH)CHO.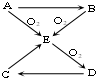 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.