题目内容
把2mL 0.1mol?L-1的H2SO4加水稀释成2L溶液,把此溶液中由水电离产生的c(H+)接近于 mol?L-1.
考点:pH的简单计算,水的电离
专题:电离平衡与溶液的pH专题
分析:依据稀释后的溶液中溶质不变,溶液中离子积Kw=c(H+)c(OH-),计算得到溶液中由水电离产生的H+.
解答:
解:把2mL 0.1mol/L的H2SO4加水稀释成2L溶液,依据溶质物质的量不变得到,稀释后的溶液浓度为
=0.0001mol/L,溶液中氢离子浓度=0.0002mol/L;酸溶液中,抑制水的电离,可忽落水电离的氢离子,可认为溶液中氢离子浓度即为酸电离的氢离子浓度,依据溶液中离子积Kw=c(H+)(酸)×c(OH-)(水)=10-14;得到溶液中由水电离产生的c(H+)(水)=c(OH-)(水)=
=5×10-11mol/L,
故答案为:5×10-11.
| 0.002L×0.1mol/L |
| 2L |
| 10-14 |
| 0.0002 |
故答案为:5×10-11.
点评:本题考查了溶液稀释后浓度的计算,溶液中离子积的计算应用,题目较简单.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
下列有关实验操作或判断正确的是 ( )
| A、用10mL量筒准确量取稀硫酸溶液8.0mL |
| B、用湿润的pH试纸测定氨水的pH |
| C、实验室制备乙烯气体时,将温度计水银球置于混合溶液的液面上方 |
| D、将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体 |
| E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫石棉网. |
常温时,将500mL pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法错误的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a) g CuCO3 |
| B、?b<a<7 |
| C、阳极电极反应:2H2O-4e-═O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |

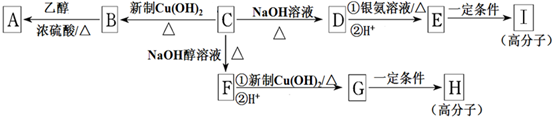
 ,满足上述条件的除A外还有
,满足上述条件的除A外还有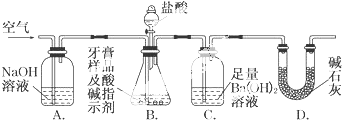
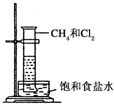 某课外兴趣小组利用如图装置探究甲烷与氯气的反应.根据题意,回答下列问题:
某课外兴趣小组利用如图装置探究甲烷与氯气的反应.根据题意,回答下列问题: