题目内容
下列说法不正确的是( )
| A、在标准状况下,NA个任何分子所占的体积约为22.4L |
| B、6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14:l |
| C、在标准状况下,总质量为28g的N2和CO的混合气体,其体积约为22.4L |
| D、磷酸的摩尔质量(以g/mol为单位)与6.02×1023个磷酸分子的质量(以g为单位)在数值上相等 |
考点:物质的量的相关计算
专题:计算题
分析:A、公式V=n?Vm只适用于气体;
B、根据n=
和m=n×M来计算;
C、根据N2和CO的摩尔质量均为28g/mol来分析;
D、一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量.
B、根据n=
| N |
| NA |
C、根据N2和CO的摩尔质量均为28g/mol来分析;
D、一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量.
解答:
解:A、公式V=n?Vm只适用于气体,故在标准状况下,只有NA个任何气体分子所占的体积才约为22.4L,故A错误;
B、6.02×1023个氮分子和6.02×1023个氢分子的物质的量均为n=
=
=1mol,而氮气的质量m═n×M=1mol×28g/mol=28g;氢气的质量m=n×M=1mol×2g/mol=2g,故两者的质量比为14:1,故B正确;
C、N2和CO的摩尔质量均为28g/mol,故28g的N2和CO的混合气体,无论N2和CO的体积分数如何变化,混合气体的物质的量一直为1mol,在标况下,体积为22.4L,故C正确;
D、一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量,故D正确.
故选A.
B、6.02×1023个氮分子和6.02×1023个氢分子的物质的量均为n=
| N |
| NA |
| 6.02×1023 |
| NA |
C、N2和CO的摩尔质量均为28g/mol,故28g的N2和CO的混合气体,无论N2和CO的体积分数如何变化,混合气体的物质的量一直为1mol,在标况下,体积为22.4L,故C正确;
D、一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量,故D正确.
故选A.
点评:本题考查了有关阿伏伽德罗常数的计算,熟练掌握公式的使用和物质的结构是解题的关键.难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
容积固定的密闭容器中,达平衡的可逆反应2A(g)?2B+C (△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是( )
| A、B和C可能都是液体 |
| B、B和C肯定都是气体 |
| C、B和C可能都是固体 |
| D、若C为固体,则B一定是气体 |
下列叙述中,不能用平衡移动原理解释的是( )
| A、红棕色的NO2,加压后颜色先变深后变浅 |
| B、高压比常压有利于合成SO3的反应 |
| C、淡黄绿色的氯水光照后颜色变浅 |
| D、由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
除去二氧化碳中混有的少量氯化氢气体,可选的试剂是( )
| A、酸性高锰酸钾溶液 |
| B、NaOH溶液 |
| C、饱和NaHCO3溶液 |
| D、石灰水 |
为提纯下列物质(括号内的物质为为杂质),所选用的除杂试剂和分离方法都正确的是( )
| 被提纯物质 | 除杂试剂 | 分离方法 | |
| A | 苯(苯甲酸) | 生石灰 | 蒸馏 |
| B | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| C | 乙烷(乙炔) | 酸性高锰酸钾溶液 | 洗气 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
| A、A | B、B | C、C | D、D |
海藻中含有丰富的碘元素.下图是实验室从海藻里提取碘的流程的一部分.下列判断正确的是( )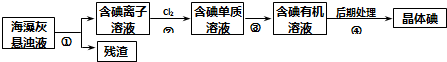

| A、步骤④的操作是过滤 |
| B、可用淀粉溶液检验步骤②的反应是否进行完全 |
| C、步骤①、③的操作分别是过滤、萃取 |
| D、步骤③中加入的有机溶剂可能是苯或CCl4 |
有机物A的结构简式为 它的同分异构体属于酚类的共有( )
它的同分异构体属于酚类的共有( )
 它的同分异构体属于酚类的共有( )
它的同分异构体属于酚类的共有( )| A、2种 | B、3种 | C、4种 | D、5种 |
下列实验操作中,能达到实验目的是( )
| A、用10mL量筒量取5.20mL盐酸 |
| B、用托盘天平称取25.20g氯化钠 |
| C、用广泛pH试纸测得溶液的pH为4.2 |
| D、用25.00mL碱式滴定管量取14.80mL NaOH溶液 |

