��Ŀ����
��ҵ�ϳ������÷�Ӧ���������������飬���ǰ��渱��Ӧ�ڡ�
��C2H4(g)+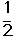 O2(g) ��
O2(g) ��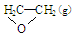 ; ��H1 ��C2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g); ��H2
; ��H1 ��C2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g); ��H2
��1��д������������ȼ�յ��Ȼ�ѧ��Ӧ����ʽ����____________________________��
��2����ҵ�����У���ͨ��ijһ��ʩ���ӿ췴Ӧ�ٶ��Է�Ӧ��Ӱ���С���Ӷ���������������Ч�ʡ���ҵ������ȡ�����ִ�ʩ��_______________��
A�����߷�Ӧ��ϵ���¶�B��������ϵ��������Ũ��
C��ʹ�ú��ʵĴ���D�����ͷ�Ӧ��ϵ��ѹǿ
��3����֪C=C��O=O��C��C���ֱܷ�Ϊa kJ��mol-1��b kJ��mol-1��c kJ��mol-1������������C��O����Ϊ kJ��mol-1��
��4����Ӧ�ڿ�����Ƴ�ȼ�ϵ�أ����������������Һ��������Ӧʽ�� ��
��1��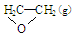 ��2.5 O2(g) =" 2" CO2 (g) +2 H2O(g) ��H=��H2-��H1 ��2��C
��2.5 O2(g) =" 2" CO2 (g) +2 H2O(g) ��H=��H2-��H1 ��2��C
��3��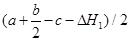 ��4��C2H4 - 12e- + 4 H2O =" 2" CO2 +12 H+
��4��C2H4 - 12e- + 4 H2O =" 2" CO2 +12 H+
���������������1���ڣ��١������ɵû���������ȼ�յ��Ȼ�ѧ��Ӧ����ʽ��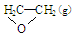 ��2.5 O2(g) =" 2" CO2 (g) +2 H2O(g) ��H=��H2-��H1����2�����ڢٵ�����Ӧ�Ǹ����������С�ķ��ȷ�Ӧ�������Ǹ������������ķ��ȷ�Ӧ��A�����߷�Ӧ��ϵ���¶�,�١���������Ӧ���ʶ��ӿ졣���������⡣����B��������ϵ��������Ũ��,���ڷ�Ӧ���Ũ���������Է�Ӧ���ʶ��ӿ졣���������⡣����C������ֻ�ܶ�ijһ��Ӧ����Ӱ�죬����������Ӧû��Ӱ�졣����ʹ�ú��ʵĴ������ܼӿ췴Ӧ�ٶ��Է�Ӧ��Ӱ���С���Ӷ���������������Ч�ʡ��������⣬��ȷ��D�����ͷ�Ӧ��ϵ��ѹǿ������������Ӧ������Ũ�ȶ���С�����Է�Ӧ���ʶ�������������ȷѡ��ΪC����3����Ӧ�Ⱦ��Ƕϼ����յ��������γɼ��ͷŵ������IJ�ֵ����C=C��O=O��C��C���ֱܷ�Ϊa kJ��mol-1��b kJ��mol-1��c kJ��mol-1������٣������ɵû���������C��O����Ϊ
��2.5 O2(g) =" 2" CO2 (g) +2 H2O(g) ��H=��H2-��H1����2�����ڢٵ�����Ӧ�Ǹ����������С�ķ��ȷ�Ӧ�������Ǹ������������ķ��ȷ�Ӧ��A�����߷�Ӧ��ϵ���¶�,�١���������Ӧ���ʶ��ӿ졣���������⡣����B��������ϵ��������Ũ��,���ڷ�Ӧ���Ũ���������Է�Ӧ���ʶ��ӿ졣���������⡣����C������ֻ�ܶ�ijһ��Ӧ����Ӱ�죬����������Ӧû��Ӱ�졣����ʹ�ú��ʵĴ������ܼӿ췴Ӧ�ٶ��Է�Ӧ��Ӱ���С���Ӷ���������������Ч�ʡ��������⣬��ȷ��D�����ͷ�Ӧ��ϵ��ѹǿ������������Ӧ������Ũ�ȶ���С�����Է�Ӧ���ʶ�������������ȷѡ��ΪC����3����Ӧ�Ⱦ��Ƕϼ����յ��������γɼ��ͷŵ������IJ�ֵ����C=C��O=O��C��C���ֱܷ�Ϊa kJ��mol-1��b kJ��mol-1��c kJ��mol-1������٣������ɵû���������C��O����Ϊ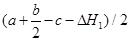 ����4�����ѷ�ӦC2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g)��Ƴ�ԭ��ء���ͨ��C2H4�ĵ缫Ϊ������ͨ��O2�ĵ缫Ϊ��������Ϊ���������������Һ�����Ը�����Ӧʽ��C2H4 - 12e- + 4 H2O =" 2" CO2 +12 H+�������ĵ缫ʽ��O2 +4e-+ 4H+= 2H2O.
����4�����ѷ�ӦC2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g)��Ƴ�ԭ��ء���ͨ��C2H4�ĵ缫Ϊ������ͨ��O2�ĵ缫Ϊ��������Ϊ���������������Һ�����Ը�����Ӧʽ��C2H4 - 12e- + 4 H2O =" 2" CO2 +12 H+�������ĵ缫ʽ��O2 +4e-+ 4H+= 2H2O.
���㣺�����Ȼ�ѧ����ʽ����д����������Ի�ѧ��Ӧ���ʵ�Ӱ�졢��Ӧ������ܵĹ�ϵ��ԭ��ص���ơ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д��о���Աͨ���Ա�������PM2��5�Ļ�ѧ����о����֣�����β����ȼú��Ⱦ�ֱ� ռ4����l8��
I����1�����ھ�������β���ķ�ӦΪ��2NO(g)+2CO(g) 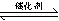 2CO2(g)+N2(g)����֪�÷�Ӧ��570Kʱ��ƽ�ⳣ��Ϊ1��1059������Ӧ���ʼ���������˵����ȷ���ǣ�
2CO2(g)+N2(g)����֪�÷�Ӧ��570Kʱ��ƽ�ⳣ��Ϊ1��1059������Ӧ���ʼ���������˵����ȷ���ǣ�
| A��װ��β������װ�õ������ų��������в��ٺ���NO��CO |
| B�����β������Ч�ʵ����;����ʹ�ø�Ч���� |
| C������ѹǿ������ƽ�����ƣ���ʵ�ʲ����п�ͨ����ѹ�ķ�ʽ����侻��Ч�� |
| D�����β������Ч�ʵij��÷����������¶� |
 N2(g)+CO2(g)
N2(g)+CO2(g)  H=akJ��mol-1����ij�ܱ���������һ�����Ļ���̿��NO������(T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
H=akJ��mol-1����ij�ܱ���������һ�����Ļ���̿��NO������(T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�| Ũ��/mol��L-1 ʱ��/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.050 | 0.025 | 0.025 |
| 30 | 0.050 | 0.025 | 0.025 |
| 40 | 0.036 | 0.032 | 0.010 |
| 50 | 0.036 | 0.032 | 0.010 |
��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K= (������λС��)��
��ǰ10min����v(NO)��ʾ�Ļ�ѧ��Ӧ����Ϊ ��30min�ı�ijһ��������Ӧ���´ﵽƽ�⣬��ı������������ ��
����30min�������¶���T2�棬�ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ3��1��l����÷�Ӧ��a 0(�>������=����<��)��
��CO���������滷����Ӱ��ܴ�CO�����������ڵ��������ȵ����⡣
��1����ҵ�ϳ���SO2��ȥCO��������ΪS��CO2����֪��ط�Ӧ���̵������仯��ͼ��ʾ
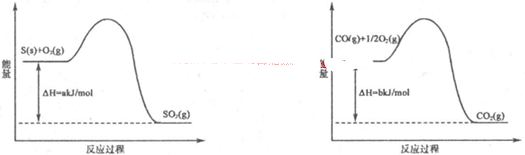
����SO2��ȥCO���Ȼ�ѧ����ʽΪ ��
��2������ʱ��Ҳ������CO��ԭMgSO4���Ʊ��ߴ�MgO��
��750��ʱ����������к������ʵ���SO2��SO3���˷�Ӧ�Ļ�ѧ����ʽ�� ��
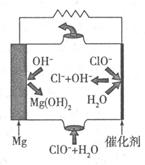
����Mg���Ƴɡ�þһ�������Ρ���أ���װ��ʾ��ͼ��ͼ����þ�缫�����ĵ缫��ӦʽΪ ���õ���ܷ�Ӧ�����ӷ���ʽΪ ��
��Ȼ�������͡�ú��������ˮ��Ӧ�Ƶ��������±���ij�ϳɰ������ò�ͬԭ��ʱ�����Ͷ�ʷ��ú��������ĵ����ݡ�
| ԭ�� | ��Ȼ�� | ���� | ú |
| ���Ͷ�ʷ��� | 1.0 | 1.5 | 2.0 |
| ��������/J��t��1 | 28��109 | 38��109 | 48��109 |
��ش��������⡣
(1)�����ϱ���Ϣ������Ϊ����________Ϊԭ����á�
(2)��д�������ڸ��¡���������������ˮ������Ӧ����������һ����̼�Ļ�ѧ����ʽ��
____________________________________________
(3)��֪C(s)��CO(g)��H2(g)��ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
C(s)��O2(g)=CO2(g)����H����394 kJ��mol��1��
2CO(g)��O2(g)=2CO2(g)����H����566 kJ��mol��1��
2H2(g)��O2(g)=2H2O(g)����H����484 kJ��mol��1��
��д����C��ˮ�����ڸ��������·�Ӧ����������һ����̼���Ȼ�ѧ����ʽ��__________________________________��
(16��)̼������������������Ҫ�ķǽ���Ԫ�ء�
��1��CH4(g)��O2(g)��ȼ������CO(g)��H2O(g)�ġ�H����ֱ�Ӳ�����ԭ���� ��
��֪��a��2CO(g)+O2(g)=2CO2(g) ��H =-566��0 kJ��mol-1
b��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H =-890��0 kJ��mol-1
��CH4(g)��O2(g)��ȼ������CO(g)��H2O(g)���Ȼ�ѧ����ʽΪ ��
��2����ҵ�Ϻϳɰ����ķ�ӦΪ��N2(g)+3H2(g)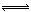 2NH3(g) ��H<0���ֽ�10 mol N2��26 mol H2�����ݻ��ɱ���ܱ������У�N2��ƽ��ת����(
2NH3(g) ��H<0���ֽ�10 mol N2��26 mol H2�����ݻ��ɱ���ܱ������У�N2��ƽ��ת����(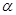 )����ϵ��ѹǿ(P)���¶�(T)�Ĺ�ϵ��ͼ��ʾ���ش��������⣺
)����ϵ��ѹǿ(P)���¶�(T)�Ĺ�ϵ��ͼ��ʾ���ش��������⣺
�ٷ�Ӧ�ﵽƽ��״̬Bʱ���������ݻ�10 L����T1ʱ���ϳɰ���Ӧ��ƽ�ⳣ��K= L2��mol-1��
��ƽ��״̬��A�䵽Cʱ����Ӧ��ƽ�ⳣ��K(A) K(C)(�>������<����=��)��
��3����25��ʱ��HSCN��HClO��H2CO3�ĵ��볣�����±���
| HClO | HSCN | H2CO3 |
| K=3.210-8 | K=0.13 | Kl=4.210-7 K2=5.610-11 |
��1 mol��L-1��KSCN��Һ�У��������ӵ�Ũ���ɴ�С��˳��Ϊ > > > ��
����Na2CO3��Һ�м������HClO��Һ����Ӧ�Ļ�ѧ����ʽΪ ��
��25��ʱ��Ϊ֤��HClOΪ���ᣬijѧϰС���ͬѧû������������ʵ�鷽�����������ַ����У�����Ϊ�ܹ��ﵽʵ��Ŀ�ĵ��� (�����и��������)��
a����pH�Ʋ���0��1 mol��L-1NaClO��Һ��pH�������pH>7����֤��HClOΪ����
b����pH��ֽ����0��01 mol��L-1HClO��Һ��pH�������pH>2����֤��HClOΪ����
c������������Ũ�Ⱦ�Ϊ0��1 mol��L-1��HClO��Һ������ĵ����ԣ������HClO��Һ�ĵ������������ᣬ��֤��HClOΪ����
��Ϊ��������ʵʩ�ġ��������䡱�����յ�վ�����Ϻ����ı���ú��ʯ��Ϊ������Դ�ṹ����Խ�����л�����Ⱦ�����ش�
(1)Ŀǰ�Ϻ��ֳ��о�����ʹ�õ�ȼ����Ҫ�ǹܵ�ú�����ֶ���������
��ʼʹ�ö�����Ȼ����Ϊ����ȼ�ϣ��ܵ�ú������Ҫ�ɷ���CO��H2������
���࣬��Ȼ������Ҫ�ɷ���CH4������ȼ�յĻ�ѧ����ʽΪ��
2CO��O2 2CO2��2H2��O2
2CO2��2H2��O2 2H2O��CH4��2O2
2H2O��CH4��2O2 CO2��2H2O
CO2��2H2O
�������ϻ�ѧ����ʽ�жϣ�ȼ����ͬ����Ĺܵ�ú������Ȼ�������Ŀ�������ϴ�����������������ȼ�չܵ�ú����������������Ȼ������ߵĸĽ������������������(�����С��)���粻���Ľ����ܲ����IJ����������������������������������������
(2)�ܵ�ú���к��е����࣬�������⣬�����������顢���顢����ȣ����ǵ�ijЩ�������£�
| | ���� | ���� | ���� |
| �۵�/�� | ��183.3 | ��189.7 | ��138.4 |
| �е�/�� | ��88.6 | ��42.1 | ��0.5 |
�Ը�������ij���ؼ����ݽ��Ͷ����Ϻ��ļ�����ʱ�ܵ�ú�������С�����ҳʶ���״̬��ԭ����___________________________��
 H2O(g)����H="+44" kJ��mol-1��16 gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų�����������������kJ��
H2O(g)����H="+44" kJ��mol-1��16 gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų�����������������kJ�� 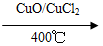 2Cl2��2H2O
2Cl2��2H2O
 SO2(g)��Cl2(g) ��H����97.3 kJ��mol��1��ij�¶�ʱ�����Ϊ1 L�ĺ����ܱ������г���0. 20mol SO2Cl2���ﵽƽ��ʱ�������к�0.18mol SO2����˹��̷�Ӧ���յ�����Ϊ_____kJ�����¶�ʱ��Ӧ��ƽ�ⳣ��Ϊ_____�����������û��������������BaCl2��Һ�У��������ɳ���������Ϊ_______��
SO2(g)��Cl2(g) ��H����97.3 kJ��mol��1��ij�¶�ʱ�����Ϊ1 L�ĺ����ܱ������г���0. 20mol SO2Cl2���ﵽƽ��ʱ�������к�0.18mol SO2����˹��̷�Ӧ���յ�����Ϊ_____kJ�����¶�ʱ��Ӧ��ƽ�ⳣ��Ϊ_____�����������û��������������BaCl2��Һ�У��������ɳ���������Ϊ_______��