��Ŀ����
(16��)̼������������������Ҫ�ķǽ���Ԫ�ء�
��1��CH4(g)��O2(g)��ȼ������CO(g)��H2O(g)�ġ�H����ֱ�Ӳ�����ԭ���� ��
��֪��a��2CO(g)+O2(g)=2CO2(g) ��H =-566��0 kJ��mol-1
b��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H =-890��0 kJ��mol-1
��CH4(g)��O2(g)��ȼ������CO(g)��H2O(g)���Ȼ�ѧ����ʽΪ ��
��2����ҵ�Ϻϳɰ����ķ�ӦΪ��N2(g)+3H2(g)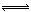 2NH3(g) ��H<0���ֽ�10 mol N2��26 mol H2�����ݻ��ɱ���ܱ������У�N2��ƽ��ת����(
2NH3(g) ��H<0���ֽ�10 mol N2��26 mol H2�����ݻ��ɱ���ܱ������У�N2��ƽ��ת����(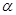 )����ϵ��ѹǿ(P)���¶�(T)�Ĺ�ϵ��ͼ��ʾ���ش��������⣺
)����ϵ��ѹǿ(P)���¶�(T)�Ĺ�ϵ��ͼ��ʾ���ش��������⣺
�ٷ�Ӧ�ﵽƽ��״̬Bʱ���������ݻ�10 L����T1ʱ���ϳɰ���Ӧ��ƽ�ⳣ��K= L2��mol-1��
��ƽ��״̬��A�䵽Cʱ����Ӧ��ƽ�ⳣ��K(A) K(C)(�>������<����=��)��
��3����25��ʱ��HSCN��HClO��H2CO3�ĵ��볣�����±���
| HClO | HSCN | H2CO3 |
| K=3.210-8 | K=0.13 | Kl=4.210-7 K2=5.610-11 |
��1 mol��L-1��KSCN��Һ�У��������ӵ�Ũ���ɴ�С��˳��Ϊ > > > ��
����Na2CO3��Һ�м������HClO��Һ����Ӧ�Ļ�ѧ����ʽΪ ��
��25��ʱ��Ϊ֤��HClOΪ���ᣬijѧϰС���ͬѧû������������ʵ�鷽�����������ַ����У�����Ϊ�ܹ��ﵽʵ��Ŀ�ĵ��� (�����и��������)��
a����pH�Ʋ���0��1 mol��L-1NaClO��Һ��pH�������pH>7����֤��HClOΪ����
b����pH��ֽ����0��01 mol��L-1HClO��Һ��pH�������pH>2����֤��HClOΪ����
c������������Ũ�Ⱦ�Ϊ0��1 mol��L-1��HClO��Һ������ĵ����ԣ������HClO��Һ�ĵ������������ᣬ��֤��HClOΪ����
��1����5�֣����Կ��Ʒ�Ӧֻ����CO(g)��2�֣����ַ�Ӧ���Կ��Ƽ��ɣ�
2CH4(g)+3O2(g)=2CO(g)+4H2O(g) ?H=��1214.0kJ?mol?1��3�֣�
��2����4�֣���0.025��2�֣��� > ��2�֣�
��3����7�֣��� c(K+)>C(SCN?)>c(OH?)>c(H+)��2�֣��������Ʒ֣�
��Na2CO3 + HClO = NaHCO3 +NaClO��3�֣�
��ac��2�֣�
���������������1��CH4ȼ����������CO2�����Կ��Ʒ�Ӧֻ����CO(g)������д��CH4��O2��Ӧ����CO��H2O�Ļ�ѧ����ʽ����ע��״̬��Ȼ����ݸ�˹��������ʱ䣺?H=��?H1+2?H2=��1214.0kJ?mol?1��������д���Ȼ�ѧ����ʽ��
��2���ٷ�Ӧ�ﵽƽ��״̬Bʱ��N2��ת����Ϊ20%����������ʽ���м���
N2(g)+3H2(g)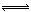 2NH3(g)
2NH3(g)
��ʼ���ʵ�����mol�� 10 26 0
ת�����ʵ�����mol�� 2 6 4
ƽ�����ʵ�����mol�� 8 20 4
��ƽ�ⳣ��Ϊ��K=(0.4mol?L?1)2��[0.8mol/L��(2mol?L?1)3]=0.025 L2��mol-1��
��B��N2ת���ʴ���C�㣬˵��B��ƽ�ⳣ������C��ƽ�ⳣ����A����B���¶���ͬ����ƽ�ⳣ����ͬ������K(A) > K(C)
��3����KSCNΪ����ǿ���Σ�SCN?ˮ��ʹ��Һ�ʼ��ԣ���������Ũ���ɴ�С��˳��Ϊ��c(K+)>C(SCN?)>c(OH?)>c(H+)
����ΪK1(H2CO3)>K(HClO)>K2(H2CO3)������HClO��Na2CO3��Ӧ����NaClO��NaHCO3����ѧ����ʽΪ��Na2CO3 + HClO = NaHCO3 +NaClO
��a����pH�ƿ��Բ���0��1 mol��L-1NaClO��Һ��pH�������pH>7��˵��NaClOˮ���Լ��ԣ���֤��HClOΪ���ᣬ��ȷ��b����ΪHClO����Ư���ԣ�����pH��ֽ����0��01 mol��L-1HClO��Һ��pH������c����ΪHClO������Ũ����ͬ�����������HClO��Һ�ĵ������������ᣬ��֤��HClOΪ���ᣬ��ȷ��
���㣺���⿼���Ȼ�ѧ����ʽ����д��ƽ�ⳣ�����жϺͼ��㡢������ʵĵ��롢�����ˮ�⡢����Ũ�ȱȽϡ�ʵ�鷽���ķ�����

���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á�
��1���ڹ̶��ݻ����ܱ������У��������»�ѧ��Ӧ��N2��g��+3H2��g��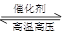 2NH3��g�� ��H=��92��4kJ/mol��
2NH3��g�� ��H=��92��4kJ/mol��
��ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T/K | 298 | 398 | 498 |
| ƽ�ⳣ��K | 4.1��106 | K1 | K2 |
���ж�K1 K2����д��>�� �� =����<������
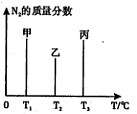
��2����2mol N2��3mol H2�ϳɰ����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�t minʱN2������������ͼ��ʾ����ʱ�ס��ҡ�������������һ���ﵽ��ѧƽ��״̬���� �����ﵽƽ��״̬ʱ��N2ת������͵��� ��
��3��NH3��CO2��120oC�����������¿��Ժϳɷ�Ӧ�������أ�CO2 +2NH3
 ��NH2��2CO +H2O
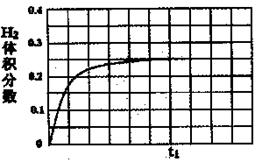
��NH2��2CO +H2O���ܱշ�Ӧ�����У����������NH3�ĺ����仯��ϵ��ͼ��ʾ
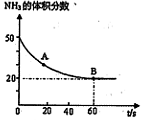
��������������Ϊ���壩����A�������Ӧ/����
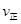 ��CO2�� B����淴Ӧ����
��CO2�� B����淴Ӧ����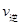 ��CO2������д��>����=����<������NH3��ƽ��ת����Ϊ____ ��
��CO2������д��>����=����<������NH3��ƽ��ת����Ϊ____ ����4����֪�����Ȼ�ѧ����ʽ��
2H2��g��+O2��g��=2H2O��1�� ��H = -571��6kJ/mol
N2��g��+O2��g��
 2NO��g�� ��H =+180kJ/mol
2NO��g�� ��H =+180kJ/mol��д����NH3��ԭNO���Ȼ�ѧ����ʽ_ ��
��5�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����д���÷�Ӧ�Ļ�ѧ����ʽ____ ����ѧ�����ô�ԭ������Ƴɰ���������ȼ�ϵ�أ���ͨ�˰����ĵ缫�� ��������������������ڼ��������£�ͨ�˰����ĵ缫�����ĵ缫��ӦʽΪ ��
 2SO3(g) ��H1 ƽ�ⳣ��ΪK1
2SO3(g) ��H1 ƽ�ⳣ��ΪK1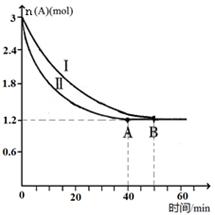
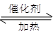 2CO2(g)+N2(g)
2CO2(g)+N2(g)
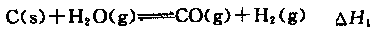


 CH3OH(g)����ƽ��ʱ�����CO��H2��CH3OH�ֱ�Ϊ1 mol��1 mol��1 mol�����������Ϊ3L�����������м���ͨ��3 mol CO����ʱv������ v���棩��ѡ���>������<������=�������жϵ����� ��
CH3OH(g)����ƽ��ʱ�����CO��H2��CH3OH�ֱ�Ϊ1 mol��1 mol��1 mol�����������Ϊ3L�����������м���ͨ��3 mol CO����ʱv������ v���棩��ѡ���>������<������=�������жϵ����� ��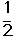 O2(g) ��
O2(g) ��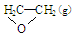 ; ��H1 ��C2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g); ��H2
; ��H1 ��C2H4(g)+3O2(g) �� 2CO2(g)+2H2O(g); ��H2