题目内容
1.将铁片和铜片用导线连接置于同一浓硝酸溶液中,下列各叙述正确的是( )
| A. | 铁片上发生氧化反应Fe-3e-═Fe3+ | B. | 铜片上发生还原反应2H++2e-═H2↑ | ||
| C. | 铜片上发生氧化反应Cu-2e-═Cu2+ | D. | 溶液中NO${\;}_{3}^{-}$的浓度基本不变 |
分析 铁与铜在浓硝酸中铁发生钝化,所以铜比铁活泼,铜失电子为负极,而铁为正极,正极的电极反应式为:2H++NO3-+e-═NO2+H2O,由此分析解答.
解答 解:A、铁为正极发生还原反应,电极反应式为:2H++NO3-+e-═NO2+H2O,故A错误;
B、铜是负极发生氧化反应,电极反应式为:Cu-2e-═Cu2+,故B错误;
C、铜是负极发生氧化反应,电极反应式为:Cu-2e-═Cu2+,故C正确;
D、正极发生还原反应,电极反应式为:2H++NO3-+e-═NO2+H2O,所以硝酸根离子浓度减少,故D错误;
故选C.
点评 本题考查了原电池的反应原理的应用,电极反应、电极判断,题目较简单.

练习册系列答案
相关题目
12.下列苯的同系物中,苯环上的一溴化物只有一种的是( )
| A. | 乙苯 | B. | 邻二甲苯 | C. | 间二甲苯 | D. | 对二甲苯 |
9.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1NaOH溶液:K+、NH4+、I-、NO3- | |
| B. | 0.1 mol•L-1的CH3COOH溶液:CH3CH2OH、Na+、Al3+、SO42- | |
| C. | 0.1 mol•L-1的Na2CO3溶液:K+、Al3+、NO3-、Cl- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1012的溶液:Fe2+、Na+、Cl-、NO3- |
6. 物质A~E在水中电离产生下列离子:
物质A~E在水中电离产生下列离子:
常温下将各物质的溶液从1ml稀释到1000ml,PH的变化关系如图所示,期中A和D反应生成E.请回答下列问题
(1)根据PH的变化关系,写出下列物质的化学式:BNaOH DCH3COOH
(2)写出A与C反应的离子方程式NH3+H+=NH4+
(3)25℃时0.1mol/L的NH4Cl溶液的PH=a,则NH4Cl溶液中c(H+)-c(NH3•H2O)=c(OH-)(用含a的关系式表示)
(4)H2SO4的酸式盐NH4HSO4,在NH4HSO4溶液中加入NaOH使溶液呈中性,则溶液中各离子浓度大小顺序为C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-).
 物质A~E在水中电离产生下列离子:
物质A~E在水中电离产生下列离子:| 阳离子 | NH4+ H+ Na+ |
| 阴离子 | OH-CH3COO- SO42- |
(1)根据PH的变化关系,写出下列物质的化学式:BNaOH DCH3COOH
(2)写出A与C反应的离子方程式NH3+H+=NH4+
(3)25℃时0.1mol/L的NH4Cl溶液的PH=a,则NH4Cl溶液中c(H+)-c(NH3•H2O)=c(OH-)(用含a的关系式表示)
(4)H2SO4的酸式盐NH4HSO4,在NH4HSO4溶液中加入NaOH使溶液呈中性,则溶液中各离子浓度大小顺序为C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-).
13.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1.01×105Pa时,32 g O2和O3的混合气体所含原子数为2NA | |
| B. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| C. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| D. | 在常温常压下,22.4 LCO2含有的原子数约为3NA |
10.实验室用自来水制取蒸馏水可以采用的实验装置是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
11.下列表达式正确的是( )
| A. | NaHCO3的电离:NaHCO3═H++CO32-+Na+ | |
| B. | Na2S的水解:S2-+2H2O?H2S+2OH- | |
| C. | CH3COONH4的电离:CH3COONH4═NH4++CH3COO- | |
| D. | FeCl3的水解:Fe3++3H2O?Fe(OH)3↓+3H+ |

 .
.

 与1mol O2恰好可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
与1mol O2恰好可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式 .
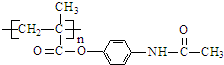
. ;扑热息痛的结构简式为
;扑热息痛的结构简式为 .
. .
.