题目内容
【化学一一选修物质结构与性质】(15分)
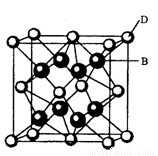
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物, D与B可形成离子化合物其晶胞结构如图所示。
请回答下列问题。
(1)E元素原子基态时的价电子排布式为 ;
(2)A2F分子中F原子的杂化类型是 ;
(3)C元素与氧形成的离子CO2-的立体构型是__________;写出一种与CO2-互为等电子体的分子的分子式________;
(4)将E单质的粉末加入CA3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是______________________________________________________;
(5)从图中可以看出,D跟B形成的离子化合物的化学式为 ;若离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (写出表达式即可)。
(1)3d104s1(2分) (2)sp3 (2分) (3)V形(2分) O3或SO2(2分)
(4)2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O(2分)
(5)CaF2(2分) (3分)
(3分)
【解析】
试题分析:有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,则A是氢元素。B是电负性最大的元素,则B是氟元素。C的2p轨道中有三个未成对的单电子,则C的核外电子排布为1s22s22p3,即C是氮元素。F原子核外电子数是B与C核外电子数之和,则F的核外电子数是16,即F是硫元素。D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,这说明E是铜。D与氟元素可形成离子化合物其晶胞结构如右图所示,根据晶胞结构可知晶胞中含有8个F原子,含有D原子的个数是8×1/8+6×1/2=4,即化学式为DF2,所以D是Ca元素。
(1)E元素的原子序数是29,则根据核外电子排布规律可知E元素原子基态时的价电子排布式为3d104s1;
(2)A2F分子是H2S,分子中S原子含有2对孤对电子,其杂化类型是sp3杂化;
(3)N元素与氧形成的离子NO2-中氮元素价层电子对数=2+(5+1-2×2)÷2=3,因此立体构型是V形;价电子数和原子数分别都相等的互为等电子体,则与CO2-互为等电子体的分子的分子式O3或SO2;
(4)将铜单质的粉末加入氨气的浓溶液中,通入O2,充分反应后溶液呈深蓝色,生成络合物,则该反应的离子方程式是2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O;
(5)根据以上分析可知D跟B形成的离子化合物的化学式为CaF2;若离子化合物晶体的密度为ag·cm-3,则 ,所以晶胞的体积是
,所以晶胞的体积是 。
。
考点:考查物质与结构性质的分析和判断

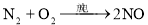
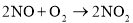
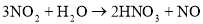

 Si(s)+4HCl(g) △H= Q kJ/mol (Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) △H= Q kJ/mol (Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是 2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。 Ni(OH)2+M
Ni(OH)2+M
 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0