��Ŀ����
�������繤ҵ���õķ�չ���˿ڵľ�����ȫ����Դ���ż�������������Խ��Խ���ص����⣬��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӡ�
��1����ͼΪC����������ı仯��ϵͼ�����ٱ仯���û���Ӧ�����仯ѧ����ʽ��Ϊ______________________________________��
ͼ�б仯������Щ�����ȷ�Ӧ________������ţ���
��2���״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ�Ͽ������·����ϳɼ״���
����һ��CO��g����2H2��g��??CH3OH��g��
��������CO2��g����3H2��g��??CH3OH��g����H2O��g��
��25�桢101 kPa�£�1�˼״���ȫȼ�շ���22.68 kJ��д���״�ȼ�յ��Ȼ�ѧ����ʽ��_____________________________________________��
ij�������糧CO2������ŷ�����2 200��֣�������CO2��ȫת��Ϊ�״������������ɴ˻�õļ״���ȫȼ�շ���Լ��________kJ��������λ��Ч���֣���
��3��������ұ������������һ����Ӧ�ǽ�ԭ�Ͻ��ʯת����TiO2�����ʯ����2C��2Cl2����,TiCl4��2CO����֪��C��s����O2��g��=CO2��g������H����393.5 kJ��mol��1
2CO��g����O2��g��=2CO2��g������H����566 kJ��mol��1
TiO2��s����2Cl2��g��=TiCl4��s����O2��g������H����141 kJ��mol��1
��TiO2��s����2Cl2��g����2C��s��=TiCl4��s����2CO��g���Ħ�H��________��
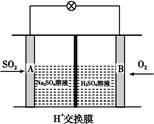
��4�����������ھ�������������ˮ������������ҵ�������ΪƯ�����������������������ҿ������������е��ʷ�Ӧ���磺
6Ag��s����O3��g��=3Ag2O��s������H����235.8 kJ��mol��1��
��֪��2Ag2O��s��=4Ag��s����O2��g����H����62.2 kJ��mol��1��
��O3ת��ΪO2���Ȼ�ѧ����ʽΪ_________________________��
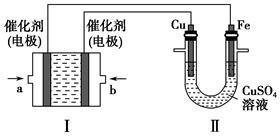
��1��C��H2O��g������,H2��CO���������ɣ�����CuO��FeO��SiO2�ȷ�Ӧ�����٢�
��2��CH3OH��l����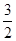 O2��g��=CO2��g����2H2O��l������H����725.76 kJ��mol��1��3.63��1014
O2��g��=CO2��g����2H2O��l������H����725.76 kJ��mol��1��3.63��1014
��3����80 kJ��mol��1
��4��2O3��g��=3O2��g������H����285 kJ��mol��1
����

 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�̼���������ĵ��ʼ��仯�����ڹ�ũҵ����������������Ҫ���á�
��1�����̼�Ȼ�ԭһ�Ȼ�����ʵ���������Ʊ�������������ص��Ȼ�ѧ����ʽ���£�
2Al2O3��s��+ 2AlCl3��g��+ 6C��s����6AlCl��g��+ 6CO��g������H�� a kJ?mol-1
3AlCl��g���� 2Al��l��+ AlCl3��g������H�� b kJ?mol-1
��ӦAl2O3��s��+ 3C��s���� 2Al��l��+ 3CO��g���ġ�H�� kJ?mol-1
���ú�a��b�Ĵ���ʽ��ʾ����
��2���û���̿��ԭ�����Դ����������ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO��������ӦC��s��+ 2NO��g��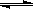 N2��g��+ CO2��g������H= Q kJ?mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
N2��g��+ CO2��g������H= Q kJ?mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
| ʱ�䣨min�� Ũ�ȣ�mol/L�� | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1��00 | 0��68 | 0��50 | 0��50 | 0��60 | 0��60 |
| N2 | 0 | 0��16 | 0��25 | 0��25 | 0��30 | 0��30 |
| CO2 | 0 | 0��16 | 0��25 | 0��25 | 0��30 | 0��30 |
��0��10min�ڣ�NO��ƽ����Ӧ����v��NO��= ��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������ ������ĸ��ţ�
a��ͨ��һ������NO b������һ�����Ļ���̿
c��������ʵĴ��� d���ʵ���С���������
����30min�������¶���T2�棬�ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ3��1��1����Q 0���������������
���ں��ݾ��������£����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬�������� ����ѡ���ţ�
a����λʱ��������2nmol NO��g����ͬʱ����nmol CO2��g��
b����Ӧ��ϵ���¶Ȳ��ٷ����ı�
c�����������ܶȲ��ٷ����ı�
��ѧ��Ҫ�о���̼Ԫ�ؼ��仯������صĺܶ���⡣
��1����̿��������ȡˮú�������12g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131. 6kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��_________ ��
��2����ҵ�Ͽ��ý�̿ұ����������0.5mol̼��ȫ�������Ӧ���õ�0.6mol����ͬʱ����2�ֳ������壬��÷�Ӧ�Ļ�ѧ����ʽ��_________��
��3��̼��ˮ������ˮú���ķ�Ӧ��һ�����淴Ӧ��������������жϸ÷�Ӧһ���ﵽƽ��״̬����_________��ѡ���ţ�����
| A��V��(H2O)=V��(H2) |
| B���������¶Ȳ��ٷ����ı� |
| C������nmolH2ͬʱ����nmolCO |
| D������������������ʵ�������ʱ��ı� |
 CO(g)+H2(g)��ƽ�ⳣ������ֵΪ_________���ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬������ͼ�л�����5���ӵ�9���Ӻ�c(H2O)Ũ�ȱ仯���Ƶ����ߣ�ֻҪ���Ա�ʾ����
CO(g)+H2(g)��ƽ�ⳣ������ֵΪ_________���ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬������ͼ�л�����5���ӵ�9���Ӻ�c(H2O)Ũ�ȱ仯���Ƶ����ߣ�ֻҪ���Ա�ʾ����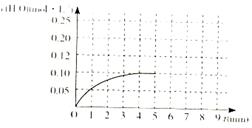
 CH3OH ( g ) ��H��-90.8 kJ��mol��1 ��һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 molH2��CO ��ƽ��ת�������¶ȣ�T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��
CH3OH ( g ) ��H��-90.8 kJ��mol��1 ��һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 molH2��CO ��ƽ��ת�������¶ȣ�T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��

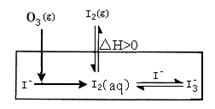
 HOI(aq) ����H2
HOI(aq) ����H2
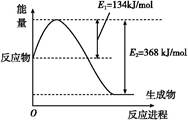
 2NO(g)����H="+179.5" kJ/mol
2NO(g)����H="+179.5" kJ/mol