题目内容
10.已知CO、CO2的混合气体的质量为15 g,在标准状况下体积为8.8 L,则可推知该混合气体中含CO4.2 g,所含CO2在标准状况下体积为5.6 L.分析 混合气体的体积为8.96L,则物质的量为$\frac{8.8L}{22.4L/mol}$=0.393mol,根据气体的总质量和总物质的量列方程式计算.
解答 解:混合气体的体积为8.96L,则物质的量为$\frac{8.8L}{22.4L/mol}$=0.393mol,
设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则28x+44y=15,x+y=0.393,
解得x=0.15mol,y=0.25mol
所以m(CO)=0.15mol×28g/mol=4.2g,
标况下0.25mol二氧化碳体积为22.4L/mol×0.1mol=5.6L,
故答案为:4.2;5.6.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力的考查,明确常见物质的摩尔质量及质量与物质的量的关系、分子的构成、阿伏伽德罗定律的推论等即可解答.

练习册系列答案
相关题目
1.下列物质中既含离子键又含共价键( )
| A. | MgCl2 | B. | NaOH | C. | CaO | D. | SO2 |
18.为提纯下列物质(括号内为杂质),所用的除杂试剂盒分离方法都正确的是( )
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4 (C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | NH4Cl溶液 (FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯 (乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | C2H5OH (H2O) | 新制生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
5.下列叙述错误的是( )
①摩尔是国际单位制中七个基本物理量之一;②1mol任何物质都含有约6.02×1023个原子;③6.02×1023就是阿伏加德罗常数;④氢原子的摩尔质量是1g;⑤HCl的摩尔质量等于1mol HCl分子的质量;⑥1mol CO2中含有1mol碳和2mol氧.
①摩尔是国际单位制中七个基本物理量之一;②1mol任何物质都含有约6.02×1023个原子;③6.02×1023就是阿伏加德罗常数;④氢原子的摩尔质量是1g;⑤HCl的摩尔质量等于1mol HCl分子的质量;⑥1mol CO2中含有1mol碳和2mol氧.
| A. | ①②③ | B. | ②③④ | C. | ②④④⑥ | D. | 全部 |
15.对于amolH2O和amolCO2的说法正确的是( )
| A. | 质量比是9:22 | B. | 相同条件下的密度一定相同 | ||
| C. | 原子个数不同 | D. | 相同条件下体积一定相同 |
2.下列说法错误的是( )
| A. | 抗酸药能中和胃里过多的盐酸,缓解胃部不适,是一类治疗胃痛的药 | |
| B. | 碳酸镁、碳酸钡都能制成抗酸药 | |
| C. | 青霉素有阻止多种细菌生长的优异功能,虽经1×107 倍稀释,仍有疗效 | |
| D. | 青霉素是重要的消炎药 |
20.在一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:C(s)+2H2O(g)?CO2(g)+2H2(g),其相关数据如表所示:
(1)T1>T2(填“>”、“<”或“=”)
(2)达到平衡后,保持温度和体积不变,向甲容器内再充入0.8molH2O和3.2molH2,则此时V正=V逆
(填“>”、“<”或“=”)
(3)在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是BD.
A.V逆(CO2)═2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均相对分子质量保持不变
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
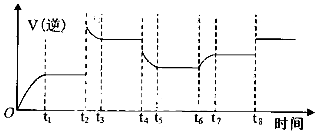
可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是通入H2O,则从t1到t8哪个时间段H2O (g)的平衡转化率最低t7-t8,(填“t1~t2,以此类推”).
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
(2)达到平衡后,保持温度和体积不变,向甲容器内再充入0.8molH2O和3.2molH2,则此时V正=V逆
(填“>”、“<”或“=”)
(3)在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是BD.
A.V逆(CO2)═2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均相对分子质量保持不变
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:

可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是通入H2O,则从t1到t8哪个时间段H2O (g)的平衡转化率最低t7-t8,(填“t1~t2,以此类推”).