题目内容
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、18g水含有电子数为8NA |
| C、标准状况下,22.4L氦气含有原子个数为NA |
| D、标准状况下,22.4 LH2O中含原子个数为3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、硫酸钠是强电解质完全电离计算;
B、依据n=
计算物质的量结合分子式计算电子数;
C、依据n
=
计算;
D、标准状况水不是气体.
B、依据n=
| m |
| M |
C、依据n
| V |
| 22.4 |
| N |
| NA |
D、标准状况水不是气体.
解答:
解:A、硫酸钠是强电解质完全电离,1mol Na2SO4溶于水中,所得溶液中Na+个数为2NA,故A错误;
B、依据n=
计算物质的量=
=1mol,结合分子式计算电子数10NA,故B错误;
C、依据n
=
计算,标准状况下,22.4L氦气含有原子个数=
×NA=NA,故C正确;
D、标准状况水不是气体,22.4L不是1mol,故D错误;
故选C.
B、依据n=
| m |
| M |
| 18g |
| 18g/mol |
C、依据n
| V |
| 22.4 |
| N |
| NA |
| 22.4L |
| 22.4L/mol |
D、标准状况水不是气体,22.4L不是1mol,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析,物质的量计算微粒数,掌握基础是关键,题目较简单.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(ClO-)=1.0mol?L-1的溶液中:Na+、SO32-、S2-、SO42- |
| B、由水电离的c(H+)=1×10-12 mol?L-1的溶液中:Ba2+、K+、Cl-、NO3- |
| C、常温下,c(H+)/c(OH-)=10-10的溶液中:Ca2+、Mg2+、HCO3-、I- |
| D、滴入少量KSCN溶液显红色的溶液中:Na+、K+、I-、SO42- |
将CO和CO2的混合气体共8L通过灼热的炭层,充分反应后恢复原状态,得到纯净的CO气体10L,则原混合气体的平均摩尔质量的数值为( )
| A、29 | B、32 | C、36 | D、40 |
用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A、标准状况下,11.2 L水中含有的原子数是1.5NA |
| B、在常温常压下,1.7g NH3含有的原子数为0.4NA |
| C、0.2mol?L-1的 K2SO4溶液中含K+数目为0.4NA |
| D、1molCl2与足量Fe反应,转移的电子数为3NA |
设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A、常温常压下,11.2LCO2所含原子数为1.5NA |
| B、常温常压下,48克O3含有的氧原子数为3NA |
| C、标准状况下,22.4L H2中所含原子数位NA |
| D、标准状况下,1LH2O所含分子数为NA/22.4 |
下列各组物质按酸、碱、盐分类顺序依次排列的是( )
| A、硫酸、纯碱、食盐 |
| B、硝酸、烧碱、生石灰 |
| C、醋酸、碱式碳酸铜、高锰酸钾 |
| D、碳酸、熟石灰、醋酸铜 |
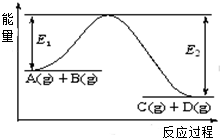 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.