题目内容
10. 已知:pKa=-lgKa,25℃时,H2SeO3的 pKa1=1.34,pKa2=7.34.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2SeO3的 pKa1=1.34,pKa2=7.34.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )| A. | a点所得溶液中:2c(H2SeO3)+c(SeO32-)<0.1 mol•L-1 | |
| B. | b点所得溶液中:c(H2SeO3)+c(H+)=c(SeO32-)+c(OH-) | |
| C. | c点所得溶液中:c(Na+)<3c(HSeO3-) | |
| D. | d点所得溶液中:c(Na+)>c(SeO32-)>c(HSeO3-) |
分析 A.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液,a点溶液中溶质为H2SeO3和NaHSeO3,PH=1.34=Pa1,则c(H2SeO3)=c(HSeO3-)依据物料守恒判断;
B.b点是用0.1mol•L-1NaOH溶液20ml滴定20mL0.1mol•L-1H2SeO3溶液,恰好反应生成NaHSeO3,溶液显酸性,依据溶液中电荷守恒和物料守恒计算分析判断;
C.c点PH=7.34=PKa2,依据平衡常数溶液显碱性,溶液中溶质主要为Na2SeO3,SeO32-+H2O?HSeO3-+OH-,Kh=$\frac{c(O{H}^{-})c(HSe{{O}_{3}}^{-})}{c(Se{{O}_{3}}^{2-})}$=$\frac{Kw}{K{a}_{2}}$,c(OH-)=$\frac{Kw}{c({H}^{+})}$,c(HSO32-)=c(SO32-),结合溶液中物料守恒分析;
D.加入氢氧化钠溶液40ml,NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液恰好反应生成Na2SeO3,d点溶液中主要是Na2SeO3和少量NaHSeO3.
解答 解:A.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液,a点溶液中溶质为H2SeO3和NaHSeO3,PH=1.34=Pa1,电离平衡常数表达式得到则c(H2SeO3)=c(HSeO3-),溶液体积大于20ml,a点所得溶液中:c(H2SeO3)+c(SeO32-)+c(HSeO3-)=2c(H2SeO3)+c(SeO32-)<0.1 mol•L-1 ,故A正确;
B.b点是用0.1mol•L-1NaOH溶液20ml滴定20mL0.1mol•L-1H2SeO3溶液,恰好反应生成NaHSeO3,溶液显酸性,溶液中电荷守恒c(Na+)+c(H+)=c(HSeO3-)+c(OH-)+2c(SeO32-),物料守恒c(Na+)=c(HSeO3-)+c(SeO32-)+c(H2SeO3),得到:c(H2SeO3)+c(H+)=c(SeO32-)+c(OH-),故B正确;
C.c点PH=7.34=PKa2,依据平衡常数溶液显碱性,溶液中溶质主要为Na2SeO3,SeO32-+H2O?HSeO3-+OH-,Kh=$\frac{c(O{H}^{-})c(HSe{{O}_{3}}^{-})}{c(Se{{O}_{3}}^{2-})}$=$\frac{Kw}{K{a}_{2}}$,c(OH-)=$\frac{Kw}{c({H}^{+})}$,c(HSeO32-)=c(SeO32-),带入计算得到:c(HSeO32-)=c(SeO32-),溶液中2n(Na)=3c(Se),2c(Na+)=3[c(SeO32-)+c(H2SeO3)+c(HSeO3-)]=3[c(H2SeO3)+2c(HSeO3-)],c(Na+)>3c(HSeO32-),故C错误;
D.加入氢氧化钠溶液40ml,NaOH溶液滴定20mL0.1mol•L-1H2SeO3溶液恰好反应生成Na2SeO3,d点溶液中主要是Na2SeO3和少量NaHSeO3,溶液中离子浓度c(Na+)>c(SeO32-)>c(HSeO3-),故D正确;
故选C.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算、离子浓度大小比较,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

| A. | 用过量石灰乳吸收工业尾气中的SO2:Ca2++2OH-+SO2═CaSO3↓+H2O | |
| B. | 用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解NaCl溶液:2C1-+2 H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| D. | 将 Fe2O3 加入到 HI 溶液中:Fe2O3+6H+═2Fe3++3 H2O |
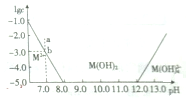
| A. | M(OH)2属于两性氢氧化物 | |
| B. | 沉淀分离M2+需控制pH在8~12之间 | |
| C. | 升高温度,可以实现从b点移动到a点 | |
| D. | 室温时,M(OH)2(s)的溶度积常数为1×10-17 |
| A. |  苯的同系物 苯的同系物 | B. |  芳香族化合物 芳香族化合物 | C. | CH3-CH═CH2烯烃 | D. |  醇 |
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A. | NaHS溶液中加入适量KOH后:c(Na+)═c(H2S)+c(HS-)+2C(S2-) | |
| B. | HCOO-、CN-、HS-在溶液中不可以大量共存 | |
| C. | 等体积、等浓度的HCOONa和NaCN两溶液中所含离子数目前者大于后者 | |
| D. | 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 |
| A. | 4.6 g NO2与N2O4的混合气体中所含氮原子数为0.1NA | |
| B. | 常温常压下1.6 g甲烷所含共用电子对数为0.1NA | |
| C. | 标准状况下,6.72 L CO2与足量NO2反应转移电子数为0.6NA | |
| D. | 50 mL 98%浓硫酸(密度为1.84 g•cm-3)与足量铜共热,转移的电子数为 0.92NA |
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
| A(g) | B2(g) | C(g) | C(g) | ||
| Ⅰ | 500 | 0.5 | 1.0 | 0 | 0.4 |
| Ⅱ | 500 | a | b | 0.25 | 0.4 |
| Ⅲ | 600 | 0.25 | 0.5 | 0.25 | 0.35 |
| A. | 容器Ⅰ中的反应在前5 min的平均反应速率v(A)=0.08 mol•L-1•min-1 | |
| B. | 该反应的正反应为放热反应 | |
| C. | 容器Ⅱ中起始时a=0.25,b=0.5 | |
| D. | 若起始时向容器Ⅰ中加入A 0.8 mol、B2 1.6 mol,达到平衡时A的转化率为80% |
