题目内容
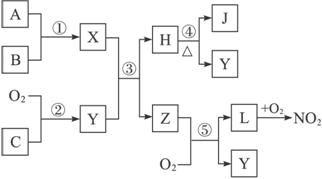
A、B、C是单质,其中A是金属,各种物质间的转化关系如图:根据图示转化关系回答:

(1)写出下列物质的化学式.A
(2)写出下列变化的化学方程式.
①A与NaOH溶液反应的化学方程式
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36L,则消耗的A的物质的量为

(1)写出下列物质的化学式.A
Al
Al
,BO2
O2
,乙NaAlO2
NaAlO2
,丁Al(OH)3
Al(OH)3
.(2)写出下列变化的化学方程式.
①A与NaOH溶液反应的化学方程式
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
.②甲与NaOH溶液反应的离子方程式Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
.(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36L,则消耗的A的物质的量为
0.1mol
0.1mol
,转移电子数目为0.3NA
0.3NA
.分析:常见金属单质中能与NaOH溶液反应产生气体的只有Al,所以A是Al,乙是NaAlO2,C是H2;甲是Al的化合物,可和NaOH溶液反应产生NaAlO2,可甲能是Al2O3,则丙是H2O,B即是O2,根据NaAlO2+CO2+2H2O═NaHCO3+Al(OH)3↓得丁是Al(OH)3,验证符合转化关系.
解答:解:常见金属单质中能与NaOH溶液反应产生气体的只有Al,所以A是Al,乙是NaAlO2,C是H2,甲是Al的化合物,可和NaOH溶液反应产生NaAlO2,甲可能是Al2O3,则丙是H2O,B即是O2,根据NaAlO2+CO2+2H2O═NaHCO3+Al(OH)3↓得丁是Al(OH)3,则:
(1)由上述分析可知,A为Al,B为O2,乙是NaAlO2,丁是Al(OH)3;
故答案为:Al,O2,NaAlO2,Al(OH)3;
(2)①Al与NaOH溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
②Al2O3与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O;
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(3)产生的H2在标准状况下的体积为3.36L,物质的量为
=0.15mol,根据2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,消耗的Al的物质的量为0.15mol×
=0.1mol,转移电子数目为0.1mol×3×NAmol-1=0.3NA;
故答案为:0.1mol,0.3NA.
(1)由上述分析可知,A为Al,B为O2,乙是NaAlO2,丁是Al(OH)3;
故答案为:Al,O2,NaAlO2,Al(OH)3;
(2)①Al与NaOH溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
②Al2O3与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O;
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(3)产生的H2在标准状况下的体积为3.36L,物质的量为
| 3.36L |
| 22.4L/mol |
| 2 |
| 3 |
故答案为:0.1mol,0.3NA.
点评:以“无机框图题”的形式考查元素单质及其化合物的性质,涉及常用化学用语与氧化还原反应等,难度中等,在熟练掌握元素化合物知识的基础上着重考查学生的发散思维、分析判断、逻辑思维以及对无机物知识的综合应用等能力,Al与碱的特殊的反应是推断的关键.

练习册系列答案
相关题目

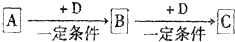 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系: