题目内容
现有铜、银合金14g与足量的某浓度的硝酸100mL发生反应,将生成的气体与1.12L(标况)氧气混合,通入足量的水中恰好全部吸收,反应后溶液体积仍为100mL.试通过计算回答下列问题:
(1)原固体混合物中铜和银的质量各是多少?
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则该反应中被还原的硝酸的物质的量是多少?
(3)合金完全溶解后,若生成的气体在标况下体积为2.24L,反应后溶液中c(H+)=7mol/L,则该混合气体中NO和NO2在标准状况下的体积分别是多少?原硝酸的浓度是多少?
(1)原固体混合物中铜和银的质量各是多少?
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则该反应中被还原的硝酸的物质的量是多少?
(3)合金完全溶解后,若生成的气体在标况下体积为2.24L,反应后溶液中c(H+)=7mol/L,则该混合气体中NO和NO2在标准状况下的体积分别是多少?原硝酸的浓度是多少?
考点:有关混合物反应的计算
专题:计算题
分析:(1)铜、银合金与足量的某浓度的硝酸完全反应,反应生成氮的氧化物与1.12L的O2(标准状况)混合,通入水中,恰好完全吸收,纵观整个过程,金属提供电子物质的量等于氧气获得电子物质的量,令Cu、Ag的物质的量分别为xmol、ymol,根据二者质量及电子转移守恒列方程解答;
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则生成气体为NO2,根据电子转移守恒计算NO2的物质的量,反应中被还原的硝酸生成NO2,根据N元素守恒计算被还原硝酸的物质的量;
(3)令NO和NO2的物质的量分别为a mol、b mol,根据二者体积及电子转移守恒列方程计算,再根据V=nVm计算各自体积;
反应后溶液中含有为硝酸铜、硝酸银及剩余的硝酸,根据电荷守恒,可知反应后溶液中n(NO3-)=n(H+)+2n(Cu2+)+n(Ag+),根据氮元素守恒可知n原溶液(HNO3)=n(NO3-)+n(NO+NO2),再根据c=
计算.
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则生成气体为NO2,根据电子转移守恒计算NO2的物质的量,反应中被还原的硝酸生成NO2,根据N元素守恒计算被还原硝酸的物质的量;
(3)令NO和NO2的物质的量分别为a mol、b mol,根据二者体积及电子转移守恒列方程计算,再根据V=nVm计算各自体积;
反应后溶液中含有为硝酸铜、硝酸银及剩余的硝酸,根据电荷守恒,可知反应后溶液中n(NO3-)=n(H+)+2n(Cu2+)+n(Ag+),根据氮元素守恒可知n原溶液(HNO3)=n(NO3-)+n(NO+NO2),再根据c=
| n |
| V |
解答:
解:(1)14g铜、银合金与足量的某浓度的硝酸完全反应,反应生成氮的氧化物与1.12L的O2(标准状况)混合,通入水中,恰好完全吸收,纵观整个过程,金属提供电子物质的量等于氧气获得电子物质的量,令Cu、Ag的物质的量分别为xmol、ymol,根据二者质量及电子转移守恒,可得:
解得x=0.05、y=0.1,
故m(Cu)=0.05mol×64g/mol=3.2g,m(Ag)=0.1mol×108g/mol=10.8g,
答:故合金中Cu的质量为3.2g、Ag的质量为10.8g.
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则生成气体为NO2,氧气的物质的量=
=0.05mol,根据电子转移守恒,故NO2的物质的量=
=0.2mol,反应中被还原的硝酸生成NO2,根据N元素守恒,被还原硝酸的物质的量等于NO2的物质的量,即被还有硝酸的物质的量为0.2mol,
答:被还有硝酸的物质的量为0.2mol;
(3)混合气体的物质的量=
=0.1mol,令NO和NO2的物质的量分别为a mol、b mol,根据二者物质的量及电子转移守恒可得:
解得a=0.05、b=0.05,
故V(NO)=V(NO2)=0.05mol×22.4L/mol=1.12L,
反应后溶液中含有为硝酸铜、硝酸银及剩余的硝酸,根据电荷守恒可知反应后溶液中n(NO3-)=n(H+)+2n(Cu2+)+n(Ag+)=0.1L×7mol/L+0.05mol×2+0.1mol=0.9mol,根据氮元素守恒可知n原溶液(HNO3)=n(NO3-)+n(NO+NO2)=0.9mol+0.1mol=1mol,故原硝酸的浓度是
=10mol/L,
答:该混合气体中NO和NO2的体积都是为1.12L,原硝酸的浓度为10mol/L.
|
解得x=0.05、y=0.1,
故m(Cu)=0.05mol×64g/mol=3.2g,m(Ag)=0.1mol×108g/mol=10.8g,
答:故合金中Cu的质量为3.2g、Ag的质量为10.8g.
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则生成气体为NO2,氧气的物质的量=
| 1.12L |
| 22.4L/mol |
| 0.05mol×4 |
| 5-4 |
答:被还有硝酸的物质的量为0.2mol;
(3)混合气体的物质的量=
| 2.24L |
| 22.4L/mol |
|
解得a=0.05、b=0.05,
故V(NO)=V(NO2)=0.05mol×22.4L/mol=1.12L,
反应后溶液中含有为硝酸铜、硝酸银及剩余的硝酸,根据电荷守恒可知反应后溶液中n(NO3-)=n(H+)+2n(Cu2+)+n(Ag+)=0.1L×7mol/L+0.05mol×2+0.1mol=0.9mol,根据氮元素守恒可知n原溶液(HNO3)=n(NO3-)+n(NO+NO2)=0.9mol+0.1mol=1mol,故原硝酸的浓度是
| 1mol |
| 0.1L |
答:该混合气体中NO和NO2的体积都是为1.12L,原硝酸的浓度为10mol/L.
点评:本题考查混合物计算、氧化还原反应的有关计算,难度中等,判断金属提供的电子等于氧气获得的电子是关键,注意氧化还原反应中守恒思想的运用.

练习册系列答案
相关题目
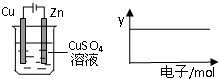 按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )| A、c(Cu2+) |
| B、c(SO42-) |
| C、Cu棒的质量 |
| D、溶液的pH |
“酸碱质子理论”认为凡是能够给出质子(H+)的分子或离子都是酸,凡是能够接受质子的分子或离子都是碱,物质酸性(碱性)的强弱取决于分子或离子给出(接受)质子能力的大小.按照“酸碱质子理论”,下列说法正确的是( )
| A、2Na+2H2O=2NaOH+H2↑是酸碱反应 |
| B、C1O-+H2O?HClO+OH-是酸碱反应 |
| C、碱性强弱顺序:ClO->OH->CH3COO- |
| D、HCO3-既是酸又是碱,NH3既不是酸又不是碱 |
 ,其分子式为
,其分子式为