题目内容
欲测定某生铁(主要成分是铁,还含有少量的碳)的组成,进行了如下实验:称取粉末状样品8.50克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体2.24L;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体1.12L.试求:(写出具体计算过程)
(1)所取盐酸的物质的量浓度.
(2)该生铁样品中碳的质量分数(保留3位有效数字).
(1)所取盐酸的物质的量浓度.
(2)该生铁样品中碳的质量分数(保留3位有效数字).
考点:有关混合物反应的计算
专题:计算题
分析:(1)由题意可知,加入的前100mL盐酸完全反应,根据n=
计算生成氢气的物质的量,根据氢元素守恒可知n(HCl)=2n(H2),再根据c=
计算;
(2)Fe完全反应生成氢气体积2.24L+1.12L=3.36L,根据n=
计算生成氢气的物质的量,根据电子转移守恒计算n(Fe),再根据m=nM计算m(Fe),进而计算碳的质量分数.
| V |
| Vm |
| n |
| V |
(2)Fe完全反应生成氢气体积2.24L+1.12L=3.36L,根据n=
| V |
| Vm |
解答:
解:(1)加入的前100mL盐酸完全反应,生成氢气的物质的量=
=0.1mol,根据氢元素守恒可知n(HCl)=2n(H2)=0.1mol×2=0.2mol,故盐酸的物质的量浓度=
=2mol/L,
答:所取盐酸的物质的量浓度为2mol/L.
(2)Fe完全反应生成氢气体积2.24L+1.12L=3.36L,生成氢气总物质的量=
=0.15mol,根据电子转移守恒,2n(Fe)=0.15mol×2,故n(Fe)=0.15mol,m(Fe)=0.15mol×56g/mol=8.4g,碳的质量=8.5g-8.4g=0.1g,故该生铁样品中碳的质量分数=
×100%=1.18%,
答:该生铁样品中碳的质量分数为1.18%.
| 2.24L |
| 22.4L/mol |
| 0.2mol |
| 0.1L |
答:所取盐酸的物质的量浓度为2mol/L.
(2)Fe完全反应生成氢气体积2.24L+1.12L=3.36L,生成氢气总物质的量=
| 3.36L |
| 22.4L/mol |
| 0.1g |
| 8.5g |
答:该生铁样品中碳的质量分数为1.18%.
点评:本题考查混合物计算,难度不大,判断Fe与盐酸反应的过量情况是关键,利用守恒思想进行解答,简化计算过程.

练习册系列答案
相关题目
在一定条件下,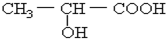 发生酯化反应,生成的酯不可能的是( )
发生酯化反应,生成的酯不可能的是( )
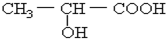 发生酯化反应,生成的酯不可能的是( )
发生酯化反应,生成的酯不可能的是( )A、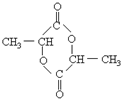 |
B、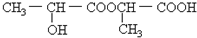 |
C、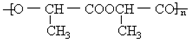 |
D、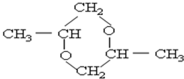 |
下列关于化学键的叙述中,正确的是( )
| A、离子化合物可能含共价键,共价化合物中不含离子键 |
| B、共价化合物可能含离子键,离子化合物中只含离子键 |
| C、阴阳离子间通过静电吸引形成的化学键叫离子键 |
| D、由非金属元素组成的化合物都是共价化合物 |
下列操作中正确的是( )
| A、除去乙烷中的少量乙烯:通入氢气,使乙烯全部转化为乙烷 |
| B、提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,取出有机层再分离 |
| C、除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层 |
| D、检验卤代烃中的卤素原子:取少量卤代烃,加入NaOH水溶液,充分加热一段时间后,在水解液中加入AgNO3溶液,观察现象 |