题目内容
20.下列说法正确的是(NA为阿伏伽德罗常数的值)( )| A. | 取1.06gNa2CO3溶于水,滴入2滴酚酞试液,用盐酸滴定至终点,所得溶液的Cl-数目约为0.01NA | |
| B. | 25℃时,将pH=2的醋酸溶液加水稀释100倍,所得溶液的H+数目约为10-4NA | |
| C. | 25℃时,向100mL1mol•L-1盐酸中通入0.1molNH3,所得溶液的H+数目为10-8NA | |
| D. | 0.1molAgCl和0.1molAgI混合后加入0.1L水中,所得溶液的c(Cl-)=c(I-) |
分析 A.1.06g碳酸钠的物质的量为0.01mol,酚酞的变色范围为8-10,滴定终点时溶质为碳酸氢钠,根据碳酸氢钠的化学式组成判断氯离子的物质的量;
B.缺少溶液体积,无法计算溶液中氢离子数目;
C.二者恰好反应生成氯化铵,铵根离子部分水解,溶液呈酸性,氢离子浓度大于10-7mol/L;
D.碘化银比氯化银更难溶,则溶液中氯离子浓度大于碘离子.
解答 解:A.1.06g碳酸钠的物质的量为:$\frac{1.06g}{106g/mol}$=0.01mol,由于酚酞的变色范围为8-10,则滴定终点时溶质为碳酸氢钠,溶液中含有氯离子的物质的量与钠离子相等,都为0.01mol,故所得溶液的Cl-数目约为0.01NA,故A正确;
B.没有告诉醋酸溶液体积,无法计算溶液中氢离子的数目,故B错误;
C.25℃时,向100mL1mol•L-1盐酸中通入0.1molNH3,反应后溶质为氯化铵,铵根离子部分水解,溶液呈酸性,氢离子浓度大于10-7mol/L,100mL该溶液中含有氢离子的物质的量大于10-8mol,所得溶液的H+数目大于10-8NA,故C错误;
D.0.1molAgCl和0.1molAgI混合后加入0.1L水中,氯化银的溶解度大于碘化银,则所得溶液的c(Cl-)>c(I-),故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,注意掌握物质的量与摩尔质量、阿伏伽德罗常数等物理量之间的转化关系,A、B为易错点,注意A滴定终点时溶质为碳酸氢钠、B中缺少溶液体积.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案
相关题目
10.高温下,某反应达平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容时,降低温度,H2 浓度增大.下列说法不正确的是( )
| A. | 该反应的焓变为正值 | |
| B. | 加入催化剂,可以增加单位体积内的活化百分子数 | |
| C. | 体积不变,冲入氦气,压强增大,化学反应速率增大 | |
| D. | 降低温度,K变小 |
11.下列物质中属于离子化合物的是( )
| A. | KOH | B. | SO3 | C. | HCl | D. | O3 |
15.以海水为原料制取下列物质时,不需要经过氧化还原反应的是( )
| A. | 溴 | B. | 铀 | C. | 氯化镁 | D. | 氢氧化钠 |
12.下列说法错误的是( )
| A. | 正丁烷和异丁烷的熔点、沸点各不相同 | |
| B. | 乙醛和丙烯醛(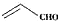 )与H2充分反应后的产物是同系物 )与H2充分反应后的产物是同系物 | |
| C. | 某有机物燃烧生成等物质的量的CO2和H2O,该有机物的通式一定为CnH2n | |
| D. | 用质谱法测定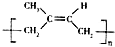 的平均相对分子质量,可得其聚合度 的平均相对分子质量,可得其聚合度 |
9.糖类、脂肪和蛋白质是维持人体生命活动所必需的营养物质,以下叙述正确的是( )
| A. | 植物通过光合作用将CO2转化成葡萄糖是太阳能转变成热能的过程 | |
| B. | 油脂属于酯类化合物,油脂可能使溴水褪色 | |
| C. | 萄糖与果糖互为同分异构体,淀粉与纤维素互为同系物 | |
| D. | 油脂、淀粉、蛋白质和维生素等均为高分子化合物 |
10.下列说法正确的是( )
| A. | 需要加热的化学反应都是不自发反应 | |
| B. | 中和反应都是放热反应 | |
| C. | 原电池是将电能转化为化学能的一种装置 | |
| D. | 太阳能电池是将化学能转化为电能的过程 |
 .
. .
.