题目内容
10.高温下,某反应达平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容时,降低温度,H2 浓度增大.下列说法不正确的是( )| A. | 该反应的焓变为正值 | |
| B. | 加入催化剂,可以增加单位体积内的活化百分子数 | |
| C. | 体积不变,冲入氦气,压强增大,化学反应速率增大 | |
| D. | 降低温度,K变小 |
分析 平衡常数指可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,平衡常数K是指可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,所以该反应化学方程式应为CO2+H2?CO+H2O;
A、恒容时,降低温度,H2 浓度增大,平衡向逆反应移动,降低温度平衡向放热反应移动;
B、加入催化剂,可以增加单位体积内的活化百分子数;
C、体积不变,充入氦气,反应物的浓度不变;
D、由A正反应是吸热反应,升高温度K值变大,降低温度K值减小.
解答 解:A、恒容时,降低温度,H2 浓度增大,平衡向逆反应移动,降低温度平衡向放热反应移动,所以正反应是吸热反应,焓变为正值,故A正确;
B、加入催化剂,可以增加单位体积内的活化百分子数,分子总数不变,故B正确;
C、体积不变,充入氦气,反应物的浓度不变,所以化学反应速率不变,故C错误;
D、由A正反应是吸热反应,升高温度K值变大,降低温度K值减小,故D正确;
故选C.
点评 本题考查化学反应速率、化学平衡、活化分子的百分数、平衡常数等,难度中等,化学反应速率和化学平衡问题一直是高考命题的热点,对化学平衡常数的考查已成为近年来高考命题的热点之一,命题主要考查的内容为求算化学平衡常数和影响因素,题目较简单.

练习册系列答案
相关题目
10.下列物质互为同分异构体的是( )
| A. | 氧气和臭氧 | B. | 正丁烷和异丁烷 | C. | 甲烷和乙烯 | D. | 1H和2H |
15. 下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
 下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )| A. | Penguinone的分子式为C10H12O | |
| B. | Penguinone的同分异构体中不可能有芳香醛 | |
| C. | Penguinone分子1mol能与3molBr2发生加成反应 | |
| D. | .Penguinone分子中所有碳原子可能处于同一平面上 |
2.1973年世界十大科技新闻中报道:中国学者许志福和美国科学家穆尔共同合成了世界上最大的碳氢分子,其中一个分子由1134个碳原子和1146个氢原子构成.关于此物质,下列说法中错误的是( )
| A. | 是烃类化合物 | B. | 常温下呈固态 | ||
| C. | 具有类似金刚石的硬度 | D. | 分子中最多可能有281个碳碳叁键 |
19.用分液漏斗可以分离的一组混合物是( )
| A. | 乙酸乙酯和乙酸 | B. | 溴苯和水 | C. | 溴乙烷和乙醇 | D. | 乙醇和水 |
20.下列说法正确的是(NA为阿伏伽德罗常数的值)( )
| A. | 取1.06gNa2CO3溶于水,滴入2滴酚酞试液,用盐酸滴定至终点,所得溶液的Cl-数目约为0.01NA | |
| B. | 25℃时,将pH=2的醋酸溶液加水稀释100倍,所得溶液的H+数目约为10-4NA | |
| C. | 25℃时,向100mL1mol•L-1盐酸中通入0.1molNH3,所得溶液的H+数目为10-8NA | |
| D. | 0.1molAgCl和0.1molAgI混合后加入0.1L水中,所得溶液的c(Cl-)=c(I-) |

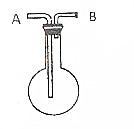 利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)
利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)
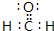 ,推测该分子的空间构型为平面三角形.
,推测该分子的空间构型为平面三角形.