题目内容
下列实验操作或对实验事实的描述正确的是 .
①用量筒量取稀硫酸溶液8.0mL;
②中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒;
③用热的浓盐酸洗涤附着有MnO2的试管;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高;
⑤Fe(OH)3胶体与FeCl3溶液可用过滤的方法分离;
⑥用碱式滴定管量得KMnO4溶液20.50mL;
⑦将水沿烧杯内壁缓缓注入浓硫酸中,不断用玻璃棒搅拌以稀释浓硫酸;
⑧用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小;
⑨锌和一定量稀硫酸反应,为加快速率而不影响H2的量可向溶液中加适量Cu(NO3)2晶体.
①用量筒量取稀硫酸溶液8.0mL;
②中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒;
③用热的浓盐酸洗涤附着有MnO2的试管;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高;
⑤Fe(OH)3胶体与FeCl3溶液可用过滤的方法分离;
⑥用碱式滴定管量得KMnO4溶液20.50mL;
⑦将水沿烧杯内壁缓缓注入浓硫酸中,不断用玻璃棒搅拌以稀释浓硫酸;
⑧用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小;
⑨锌和一定量稀硫酸反应,为加快速率而不影响H2的量可向溶液中加适量Cu(NO3)2晶体.
考点:化学实验方案的评价
专题:实验评价题
分析:①量筒感量是0.1mL;
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒;
③加热条件下,浓盐酸和二氧化锰反应生成可溶性氯化锰;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸;
⑥碱式滴定管只能盛放碱溶液;
⑦稀释浓硫酸时,浓硫酸倒入水中;
⑧用湿润的pH试纸测量某溶液pH时,导致所测溶液浓度偏低;
⑨锌和硝酸反应生成NO.
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒;
③加热条件下,浓盐酸和二氧化锰反应生成可溶性氯化锰;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸;
⑥碱式滴定管只能盛放碱溶液;
⑦稀释浓硫酸时,浓硫酸倒入水中;
⑧用湿润的pH试纸测量某溶液pH时,导致所测溶液浓度偏低;
⑨锌和硝酸反应生成NO.
解答:
解:①量筒感量是0.1mL,所以可以用量筒量取稀硫酸溶液8.0mL,故正确;
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒,因为金属棒会传递热量,导致测量结果偏小,故错误;
③热的浓盐酸和二氧化锰反应生成可溶性氯化锰,稀盐酸和二氧化锰不反应,故正确;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解,固体减少的质量增大,则所测结晶水含量可能会偏高,故正确;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸,所以不能用过滤的方法分离,应该用渗析的方法分离,故错误;
⑥高锰酸钾溶液呈酸性,只能用酸式滴定管量取,故错误;
⑦将浓硫酸沿烧杯内壁缓缓注入水中,为防止局部温度过高而溅出液体,不断用玻璃棒搅拌以稀释浓硫酸,故错误;
⑧用湿润的pH试纸测量某溶液pH时,溶液浓度偏小,导致测量不准确,故错误;
⑨锌和硝酸铜的酸性溶液反应生成NO,从而影响生成氢气的量,故错误;
故选①③④.
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒,因为金属棒会传递热量,导致测量结果偏小,故错误;
③热的浓盐酸和二氧化锰反应生成可溶性氯化锰,稀盐酸和二氧化锰不反应,故正确;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解,固体减少的质量增大,则所测结晶水含量可能会偏高,故正确;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸,所以不能用过滤的方法分离,应该用渗析的方法分离,故错误;
⑥高锰酸钾溶液呈酸性,只能用酸式滴定管量取,故错误;
⑦将浓硫酸沿烧杯内壁缓缓注入水中,为防止局部温度过高而溅出液体,不断用玻璃棒搅拌以稀释浓硫酸,故错误;
⑧用湿润的pH试纸测量某溶液pH时,溶液浓度偏小,导致测量不准确,故错误;
⑨锌和硝酸铜的酸性溶液反应生成NO,从而影响生成氢气的量,故错误;
故选①③④.
点评:本题考查了实验方案评价,涉及知识点较多,明确实验原理是解本题关键,注意⑨中隐含条件,为易错点.

练习册系列答案
相关题目
化学与日常生活联系紧密,下列说法不正确的是( )
| A、小苏打、氢氧化铝可以治疗胃酸过多症 |
| B、淡黄色粉末Na2O2可用于“蛟龙号”的供氧剂 |
| C、造成大气污染的“PM2.5”是气溶胶 |
| D、明矾净水的原理是Al3+水解生成的Al(OH)3胶体有强的吸附性 |
 氯仿(CHCl3)常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3+O2→2HCl+2COCl2.下列说法不正确的有( )
氯仿(CHCl3)常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3+O2→2HCl+2COCl2.下列说法不正确的有( )| A、CHCl3分子的空间构型为正四面体 |
| B、COCl2分子中中心C原子采用sp2杂化 |
| C、COCl2分子中所有原子的最外层电子都满足8电子稳定结构 |
| D、使用前可用硝酸银稀溶液检验氯仿是否变质 |
 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.

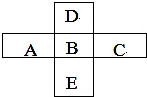 A、B、C、D、E五种主族元素所处周期表的位置如图所示.
A、B、C、D、E五种主族元素所处周期表的位置如图所示.