题目内容
下列离子方程式书写正确的是
| A.铁溶于盐酸中 2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O |
| C.二氧化硫被烧碱溶液吸收 SO2 +2OHˉ= SO32ˉ + H2O |
| D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O |
C
解析试题分析:A、违反客观事实,应为Fe2+,故错;B、电荷、质量都不守恒,故错;D、电荷不守恒,故错。故选C。
考点:离子方程式正误判断要注意:看原则:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
下列表述正确的是
A.含有大量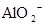 的溶液中:K+、 的溶液中:K+、 、 、 、 、 可共存 可共存 |
B.CO(g)的燃烧热是283.0kJ·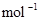 ,则 ,则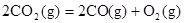 反应的 反应的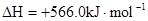 |
C.将SO2通入 溶液中: 溶液中: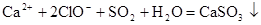 +2HClO +2HClO |
D.在某钠盐溶液中含有等物质的量的 、 、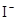 、 、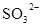 、 、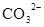 、 、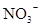 、 、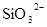 中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有 中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有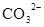 |
下列反应的离子方程式中,书写正确的是
A.氯气溶于水: |
B.将铝粉投入氢氧化钠溶液中: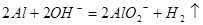 |
C.铜与氯化铁溶液反应: |
D.过氧化钠与水反应: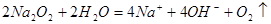 |
下列表示对应化学反应的离子方程式正确的是
| A.用白醋除铁锈:Fe2O3+6H+=3H2O+2Fe3+ |
| B.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热: Ba2++ 2OH-+NH4++ HCO3-  NH3↑+2H2O+BaCO3↓ NH3↑+2H2O+BaCO3↓ |
| C.用过量冷氨水吸收SO2:SO2+NH3·H2O=HSO3-+NH4+ |
| D.用强碱吸收工业制取硝酸尾气:NO+ NO2+2OH-=2NO3-+H2O |
下列离子方程式书写正确的是( )
A.碳酸钠溶液滴入酚酞变红: CO32- + 2H2O 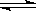 H2CO3 + 2OH- H2CO3 + 2OH- |
| B.铜溶解于氯化铁溶液中:2Fe3++3Cu=2Fe+3Cu2+ |
| C.氯化铝溶液与过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.FeSO4溶液中滴入稀硝酸:3Fe2+ + 4H+ + NO3- = 3Fe3+ + 2H2O + NO↑ |
下列说法正确的是( )
| A.强电解质一定可溶于水 |
| B.弱电解质是指部分溶于水的化合物 |
| C.弱电解质的导电性一定弱 |
| D.强酸、强碱不一定抑制弱酸弱碱的电离 |
在溶液中加入过量Na2O2后仍能大量共存的离子组是
| A.Fe2+、NH4+、Cl-、NO3- | B.K+、CO32-、Cl-、SO42- |
| C.Ca2+、Na+、NO3-、HCO3- | D.Na+、H+、Cl-、Br- |
已知I2+SO32—+H2O==2I—+SO42—+2H+。某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液的判断正确的是
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-
| A.②③④ | B.①②③ | C.①③ | D.①② |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、AlO2-、SO42- |
| C.Na+、S2-、CO32-、SO42- |
| D.Na+、Ba2+、CH3COO-、HCO3- |