题目内容
下列说法正确的是( )
| A.强电解质一定可溶于水 |
| B.弱电解质是指部分溶于水的化合物 |
| C.弱电解质的导电性一定弱 |
| D.强酸、强碱不一定抑制弱酸弱碱的电离 |
D
解析试题分析:A选项,硫酸钡为强电解质,但属于难溶物。B选项,醋酸为弱电解质,但可以和水任意比例混溶。C选项,电解质溶液的导电能力与电解质的浓度及所带电荷量有关,与电解质的强弱无关。D选项,正确。
考点:电解质

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列反应的离子方程式正确的是
| A.NaHCO3溶液与盐酸:CO32? + 2 H+ = H2O + CO2↑ |
| B.硝酸银溶液与铜:Cu + Ag+ = Cu2++ Ag |
| C.向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O |
| D.用醋酸除水垢:2CH3COOH + CaCO3 = Ca2+ + 2CH3COO? + H2O + CO2↑ |
下列离子方程式书写正确的是:
| A.氯化铝溶液和过量的氨水反应:Al3++4NH3·H2O=AlO2-+4NH4+ |
| B.少量的CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2O |
| C.醋酸加入小苏打溶液中:HCO3-+H+=CO2↑+H2O |
D.硫化钠的水解:S2-+2H2O H2S+2OH- H2S+2OH- |
下列离子方程式正确的是( )
| A.碳酸钙溶于醋酸:CaCO3+2H+= Ca2++CO2↑ +H2O |
| B.Fe3O4溶于稀盐酸:Fe3O4+8H+=3Fe3++4H2O |
| C.用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O |
| D.向硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液 : Fe2++H2O2+2H+=Fe3++4H2O |
下列离子方程式书写正确的是
| A.铁溶于盐酸中 2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O |
| C.二氧化硫被烧碱溶液吸收 SO2 +2OHˉ= SO32ˉ + H2O |
| D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O |
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
| A.氢氧化钠与盐酸;氢氧化钠与硫酸铜 |
| B.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 |
| C.Na2CO3溶液与硝酸溶液;CaCO3溶液与硝酸溶液 |
| D.石灰石与硝酸反应;石灰石与盐酸 |
在pH=13的无色溶液中,下列各组离子能大量共存的是( )
| A.K+、Na+、HCO3-、NO3- | B.Na+、NH4+、NO3-、Cl- |
| C.K+、Na+、NO3-、Br- | D.K+、Cu2+、Cl-、SO42- |
下列各组离子在指定条件下,一定能大量共存的是
| A.pH为1的无色溶液:K+、Fe2+、SO32-、Cl- |
| B.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl- |
| D.加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、SO42- |
下列各表述与示意图一致的是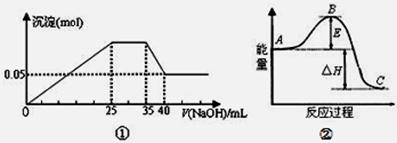
| A.图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图。则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 |
| B.图①中使用的NaOH的浓度为2mol/L |
| C.图②中曲线表示某反应过程的能量变化。若使用催化剂,B点会降低 |
| D.图②中物质A反应生成物质C,△H>0; |