��Ŀ����
14�������ϩ��һ�ֻ���ԭ�ϣ��ڹ�ҵ������������ת����ϵ��

��ش��������⣺
��1�������ϩ��ϵͳ����Ϊ2-��-1��3-����ϩ��A��B�ķ�Ӧ�������ڼӳɷ�Ӧ��B����D��E�ķ�Ӧ��������������Ӧ��
��2��B�Ľṹ��ʽ��
 ��D�ĺ˴Ź���������3��壮
��D�ĺ˴Ź���������3��壮��3��A〜G�л�Ϊͬϵ�����D��E�����л�����ĸ��ţ���
��4��F����PHB�Ļ�ѧ����ʽ��
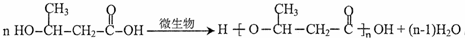 ��
����5��E��ͬ���칹���У����ܷ���������Ӧ��Ҳ����̼��������Һ��Ӧ�Ĺ���12�֣������������칹����
��6�����ձ���ת����ϵͼ������Ȳ��1��3-����ϩΪ��Ҫ�л�ԭ���Ʊ�
 �ĺϳ�·��ͼΪ
�ĺϳ�·��ͼΪ ��
�����ϳ�·��ͼ�ı�ʾ�����磬CH3CH3OH$��_{Cu����}^{O_{2}}$CH3CHO$��_{����}^{O_{2}}$CH3COOH��
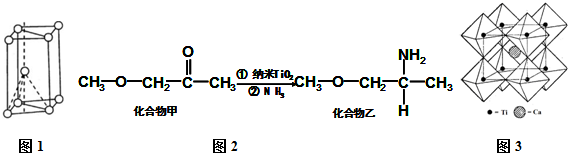
���� A��HC��CCH��CH3��2������Ϣ���еļӷ�Ӧ��B��B�������ӳɵ�C������C�Ľṹ��B�ķ���ʽ��֪BΪ ��B������Ϣ���е�������Ӧ��D��E��D�����������ӳɷ�Ӧ��FΪCH3CH��OH��CH2COOH��F�������۷�Ӧ��PHB��
��B������Ϣ���е�������Ӧ��D��E��D�����������ӳɷ�Ӧ��FΪCH3CH��OH��CH2COOH��F�������۷�Ӧ��PHB��
��� �⣺A��HC��CCH��CH3��2������Ϣ���еļӷ�Ӧ��B��B�������ӳɵ�C������C�Ľṹ��B�ķ���ʽ��֪BΪ ��B������Ϣ���е�������Ӧ��D��E��D�����������ӳɷ�Ӧ��FΪCH3CH��OH��CH2COOH��F�������۷�Ӧ��PHB��
��B������Ϣ���е�������Ӧ��D��E��D�����������ӳɷ�Ӧ��FΪCH3CH��OH��CH2COOH��F�������۷�Ӧ��PHB��
��1�������ϩ��ϵͳ����Ϊ��2-��-1��3-����ϩ��A��B�ķ�Ӧ�������ڼӳɷ�Ӧ��B����D��E�ķ�Ӧ��������������Ӧ��
�ʴ�Ϊ��2-��-1��3-����ϩ���ӳɷ�Ӧ��������Ӧ��
��2��B�Ľṹ��ʽΪ�� ��D�ķ�������3�ֻ�ѧ������ͬ����ԭ�ӣ��˴Ź���������3�����շ壬
��D�ķ�������3�ֻ�ѧ������ͬ����ԭ�ӣ��˴Ź���������3�����շ壬
�ʴ�Ϊ�� ��3��
��3��
��3������ת����ϵ�У�D��E�������������������Ŀ��ͬ����������2��CH2������D��E��Ϊͬϵ�
�ʴ�Ϊ��D��E��
��4��F����PHB�Ļ�ѧ����ʽ�ǣ�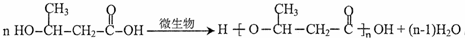 ��
��
�ʴ�Ϊ��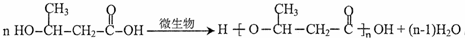 ��
��
��5��E��ͬ���칹���У����ܷ���������Ӧ��Ҳ����̼��������Һ��Ӧ��˵����ȩ�����Ȼ������Կ������鱻-CHO��-COOHȡ���������鱻ȡ��ʱ��-COOHȡ������Hԭ��ʱ��-CHO��4��λ�ã�-COOHȡ���Ǽ���Hԭ��ʱ��-CHO��4��λ�ã��춡�鱻ȡ��ʱ��-COOHȡ������Hԭ��ʱ��-CHO��3��λ�ã�-COOHȡ���μ���Hԭ��ʱ��-CHO��1��λ�ã���12�֣�
�ʴ�Ϊ��12��
��6������ϩ����Ȳ�����ӳɷ�Ӧ���� ��������ˮ�����ӳɷ�Ӧ����
��������ˮ�����ӳɷ�Ӧ���� ���������������ˮ��Һ�����������·���ˮ�ⷴӦ����
���������������ˮ��Һ�����������·���ˮ�ⷴӦ���� ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶ���ϳɣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ���������������л���ṹ�����ʽ�����ƶϣ��������չ����ŵ�������ת����֪��������Ӧ���ͼ���Ӧ������

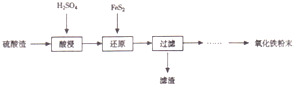
ע�����������Ҫ��Fe2O3��SiO2��Al2O3��MgO�������ʣ�
��1���������������Ҫ�ʵ�������Ŀ���ǣ���������Ľ����ʣ�������Fe3+��ˮ��
��2������ԭ���ǽ�Fe3+ת��ΪFe2+��ͬʱFeS2������ΪSO42-���÷�Ӧ�����ӷ���ʽΪ14Fe3++FeS2+8H2O=15Fe2++2SO42-+16H+
��3 ��Ϊ�ⶨ��������������Һ��Fe3+�����Կ��Ƽ���FeS2������ʵ�鲽��Ϊ��ȷ��ȡһ���������������Һ����ƿ�У�����HCl���Թ���SnCl2���ټ�HgCl2��ȥ������SnCl2�Զ�����������Ϊָʾ������K2Cr2O3����Һ�ζ����йط�Ӧ�������£�
2Fe3++Sn2++6Cl-�T2Fe2++SnCl42-
Sn2++4Cl-+2HgCl2�TSnCl42-+Hg2Cl2��
6Fe2++Cr2O32-+14H+�T6Fe3++2Cr3++7H2O
����SnCl2����������ⶨ��Fe3+��ƫ�ͣ��ƫ�ߡ�����ƫ�͡��������䡱����ͬ��
��������HgCl2����ⶨ��Fe3+��ƫ��
��4���ٿ�ѡ��KSCN��
 �����Լ���������Һ�к���Fe3+�����������Fe3+�ɱ�������O2�����������ӷ�Ӧ����ʽ��ʾ��4Fe2++O2+4H+=4Fe3++2H2O
�����Լ���������Һ�к���Fe3+�����������Fe3+�ɱ�������O2�����������ӷ�Ӧ����ʽ��ʾ��4Fe2++O2+4H+=4Fe3++2H2O����֪���������������������γɳ���ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | A1��0H��3 | Fe��OH��2 | Mg��OH��2 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| ��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
��һ������������Һ�м�����������Ը��������Һ�����裨��д���������
�ʶ����������μ�NaOH��Һ��������ҺΪpHΪ3.2��3.8����д���������
�����������룬ϴ�ӣ�
���IJ�����ɣ���ĥ��
| ��ѧ�� | H-H | F-F | H-F | H-Cl | H-1 |
| E��kJ/mol�� | 436.0 | 157 | 568 | 431.8 | 298.7 |
| A�� | �������ȶ��Ļ�ѧ����H-F | |
| B�� | 431.8 kJ/mol��E��H-Br����298.7 kJ/mol | |
| C�� | H2��g����2H��g����H=+436.0 kJ/mol | |
| D�� | H2��g��+F2��g����2HF��g����H=-25kJ/mol |
| A�� | O3 | B�� | SO2 | C�� | CO | D�� | N2 |


 ��
�� $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$ +H2O��
+H2O�� +4NaOH$��_{��}^{ˮ}$CH3CH2COONa+
+4NaOH$��_{��}^{ˮ}$CH3CH2COONa+ +2H2O+2NaCl��
+2H2O+2NaCl�� ��
��