题目内容
6.将铜片溶于稀硝酸中,发生下列反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O在上述反应中,未被还原的HNO3和被还原HNO3的个数比为( )| A. | 3:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
分析 该反应中,铜失电子作还原剂,部分硝酸作氧化剂,根据反应方程式中元素化合价变化确定参加氧化还原反应的硝酸和未参加氧化还原反应的硝酸并结合N=nNA来解答.
解答 解:反应中N元素化合价降低,HNO3为氧化剂,Cu元素化合价升高,被氧化,根据方程式可判断,当8molHNO3参加反应时,有2mol被还原,表现为氧化性,6molHNO3表现为酸性,未被还原的HNO3与被还原的HNO3物质的量之比是3:1,根据N=nNA知未被还原的HNO3和被还原HNO3的分子个数比为3:1,
故选A.
点评 本题考查氧化还原反应的计算,把握反应中物质的量的关系为解答的关键,注意8mol硝酸反应时只有2mol作氧化剂被还原为易错点,题目难度不大.

练习册系列答案
相关题目
16.中学化学中很多“规律”都有其使用范围,据有关“规律”下列结论合理的是( )
| A. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| B. | 金属钠可以通过电解熔融NaCl制得,推出金属铝可以通过电解熔融AlCl3制得 | |
| C. | 金属钠在纯氧中燃烧生成Na2O2,推出金属锂在纯氧中燃烧生成Li2O2 | |
| D. | CaCO3与稀硝酸反应生成CO2,推出CaSO3也能与稀硝酸反应生成SO2 |
17.下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋白溶液;②淀粉溶液;③硫酸钠溶液;④纯水;⑤沸水中滴入饱和FeCl3溶液;⑥肥皂水;⑦把氯化钠研磨成直径在1~100nm的颗粒然后分散于水中.
①鸡蛋白溶液;②淀粉溶液;③硫酸钠溶液;④纯水;⑤沸水中滴入饱和FeCl3溶液;⑥肥皂水;⑦把氯化钠研磨成直径在1~100nm的颗粒然后分散于水中.
| A. | ③⑦ | B. | ③④⑦ | C. | ②④ | D. | ③④ |
14.食盐、纯碱(Na2CO3)、食醋均为厨房中常用的物质,利用这些物质不能实现的实验是( )
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①② |
1.下列说法错误的是( )
| A. | 摩尔是物质的量的单位 | |
| B. | 国际上规定,0.012kg 12C原子所含有的碳原子数目的物质的量为1mol | |
| C. | mol H2的质量是2g,它所占的体积是 22.4L | |
| D. | 硫酸根离子的摩尔质量是 96g/mol |
9.下列制备和收集气体的实验装置合理的是( )
| A. |  用锌粒和稀硫酸制H2 | B. |  用H2O2和MnO2制O2 | ||
| C. | 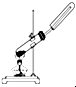 用氯化铵和氢氧化钙固体制NH3 | D. |  用铜片和稀硝酸制NO |
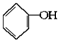 合成
合成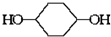 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).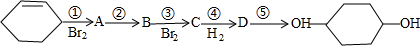
 、D
、D .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ .
.