题目内容
写出下列反应的离子方程式:
(1)三氯化铁溶液与氢氧化钠溶液反应 .
(2)铁与硫酸铜溶液反应 .
(3)少量二氧化碳通入澄清石灰水中 .
(4)铝与稀硫酸反应 .
(5)氢氧化钡溶液与硫酸铜溶液混合 .
(1)三氯化铁溶液与氢氧化钠溶液反应
(2)铁与硫酸铜溶液反应
(3)少量二氧化碳通入澄清石灰水中
(4)铝与稀硫酸反应
(5)氢氧化钡溶液与硫酸铜溶液混合
考点:离子方程式的书写
专题:离子反应专题
分析:(1)铁离子与氢氧根离子反应生成氢氧化铁沉淀;
(2)铁活泼性大于铜,铁与铜离子反应生成铜和亚铁离子;
(3)氢氧化钙与二氧化碳反应生成碳酸钙沉淀,氢氧化钙需要拆开;
(4)铝与氢离子反应生成铝离子和氢气;
(5)氢氧化钡与硫酸铜溶液反应生成硫酸钡沉淀和氢氧化铜沉淀.
(2)铁活泼性大于铜,铁与铜离子反应生成铜和亚铁离子;
(3)氢氧化钙与二氧化碳反应生成碳酸钙沉淀,氢氧化钙需要拆开;
(4)铝与氢离子反应生成铝离子和氢气;
(5)氢氧化钡与硫酸铜溶液反应生成硫酸钡沉淀和氢氧化铜沉淀.
解答:
解:(1)氯化铁溶液和氢氧化钠溶液反应生成氢氧化铁沉淀和氯化钠,反应的化学方程式为:3NaOH+FeCl3═Fe(OH)3↓+3NaCl,根据离子方程式的书写原则,该反应的离子方程式为:Fe3++3OH-═Fe(OH)3↓,
故答案为:Fe3++3OH-═Fe(OH)3↓;
(2)铁与硫酸铜溶液反应化学方程式:Fe+CuSO4=Cu+FeSO4;硫酸亚铁和硫酸铜都是易溶于水的盐,反应离子方程式为Fe+Cu2+=Cu+Fe2+,
故答案为:Fe+Cu2+=Cu+Fe2+;
(3)二氧化碳能使石灰水中的氢氧化钙反应生成碳酸钙白色沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,改写成离子方程式为:CO2+Ca2++2OH-═CaCO3↓+H2O,
故答案为:CO2+Ca2++2OH-═CaCO3↓+H2O;
(4)在金属活动顺序表中,铝排在氢的前面,所以铝与稀硫酸能反应且生成硫酸铝和氢气,反应的化学方程式为:2Al+3H2SO4═Al2(SO4)3+3H2↑,改写成离子方程式为:2Al+6H+═2Al3++3H2↑,
故答案为:2Al+6H+═2Al3++3H2↑;
(5)硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,反应的离子方程式为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓,
故答案为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓.
故答案为:Fe3++3OH-═Fe(OH)3↓;
(2)铁与硫酸铜溶液反应化学方程式:Fe+CuSO4=Cu+FeSO4;硫酸亚铁和硫酸铜都是易溶于水的盐,反应离子方程式为Fe+Cu2+=Cu+Fe2+,
故答案为:Fe+Cu2+=Cu+Fe2+;
(3)二氧化碳能使石灰水中的氢氧化钙反应生成碳酸钙白色沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,改写成离子方程式为:CO2+Ca2++2OH-═CaCO3↓+H2O,
故答案为:CO2+Ca2++2OH-═CaCO3↓+H2O;
(4)在金属活动顺序表中,铝排在氢的前面,所以铝与稀硫酸能反应且生成硫酸铝和氢气,反应的化学方程式为:2Al+3H2SO4═Al2(SO4)3+3H2↑,改写成离子方程式为:2Al+6H+═2Al3++3H2↑,
故答案为:2Al+6H+═2Al3++3H2↑;
(5)硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,反应的离子方程式为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓,
故答案为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓.
点评:本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式中必须遵循电荷守恒、质量守恒定律,还需要检查反应物、生成物的拆分是否正确.

练习册系列答案
相关题目
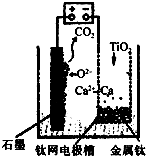 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )| A、该电池工作过程中O2-向阴极移动 |
| B、阳极的电极反应式为C+2O2--4e-═CO2↑ |
| C、若用铅蓄电池作该装置的供电电源,“-”接线柱应连接PbO2电极 |
| D、在制备金属钛前后,整套装置中CaO的总量减少 |
下列离子方程式书写正确的是( )
| A、氧化铜与盐酸反应:O2-+2H+=H2O |
| B、NaHCO3溶液与NaOH溶液反应 H++OH-=H2O |
| C、氢氧化铁胶体的制备:Fe3++3H2O=Fe(OH)3↓+3H+ |
| D、大理石溶于醋酸的反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |