题目内容
如图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有 ( )
A、 |
B、 |
C、 |
D、 |
E、 |
考点:实验装置综合,气体的收集,尾气处理装置
专题:化学实验基本操作
分析:极易溶于水的气体,若吸收时导管伸入水中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象,所以不能把导管直接深入水中,据此分析.
解答:
解:A、吸收装置中的导管没直接伸入到液体中,不易吸收气体;故A错误;
B、吸收装置中的导管外联双球状导管内伸入到液体中,能防止倒吸;故B正确;
C、吸收装置中的导管下联漏斗,漏斗完全伸入液面以下,易吸收易溶性气体,不能防止倒吸;故C错误;
D、倒置球形漏斗插入溶液中,气体能被充分吸收,且球形管有缓冲作用而防止倒吸.故D正确.
E、水的密度比四氯化碳小且水和四氯化碳不互溶,所以水浮在四氯化碳的上面,四氯化碳不能和NH3反应,也不溶解NH3,该装置既能够吸收易溶性气体,又能够防止倒吸,故E正确.
故答案为:BDE;
B、吸收装置中的导管外联双球状导管内伸入到液体中,能防止倒吸;故B正确;
C、吸收装置中的导管下联漏斗,漏斗完全伸入液面以下,易吸收易溶性气体,不能防止倒吸;故C错误;
D、倒置球形漏斗插入溶液中,气体能被充分吸收,且球形管有缓冲作用而防止倒吸.故D正确.
E、水的密度比四氯化碳小且水和四氯化碳不互溶,所以水浮在四氯化碳的上面,四氯化碳不能和NH3反应,也不溶解NH3,该装置既能够吸收易溶性气体,又能够防止倒吸,故E正确.
故答案为:BDE;
点评:本题考查了对于极易溶于水的气体的防倒吸装置,题目难度不大,注意有缓冲作用的装置能防止倒吸,侧重于基本实验装置的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某同学量取50ml 0.5mol/LNaOH溶液和30ml 0.5mol/L H2SO4溶液做中和热实验,测得中和热数据比57.3kJ?mol-1大,其原因可能是( )
| A、实验装置保温、隔热效果差 |
| B、量取NaOH溶液的体积时仰视读数 |
| C、分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D、用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
下列离子方程式书写正确的是( )
| A、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -=2Al(OH)3↓+3BaSO4↓ |
| B、向FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| C、向Ba(OH)2溶液中加入过量的NaHCO3:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32- |
| D、足量Cl2通入1.0mol?L-1 Na2SO3溶液中:2SO32-+Cl2=2S↓+2ClO3- |
下列图示实验合理的是( )
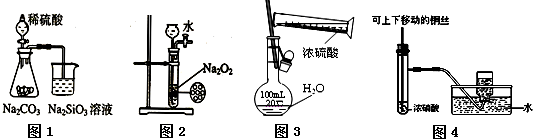

| A、图1为证明非金属性强弱:S>C>Si |
| B、图2为制备少量氧气 |
| C、图3为配制一定浓度硫酸溶液 |
| D、图4为制备并收集少量NO2气体 |
在密闭容器中,一定量混合气体发生下列反应:aM(g)+bN(g)?cW(g),达一平衡后,测得M气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L.则下列叙述正确的是( )
| A、反应速率增大 |
| B、W的体积分数降低 |
| C、N的转化率提高 |
| D、平衡向右移动 |
下列可逆反应达平衡状态后,降温可以使混和气体平均相对分子质量减小的是( )
| A、H2(气)+Br2(气)?2HBr(气) (正反应为放热反应) |
| B、N2(气)+3H2(气)?2NH3(气) (正反应为放热反应) |
| C、2SO3(气)?2SO2(气)+O2(气) (正反应为吸热反应) |
| D、4NH3(气)+5O2(气)?4NO(气)+6H2O(气) (正反应为放热反应) |
下列图象分别表示有关反应的反应过程与能量变化的关系 据此判断下列说法正确的是( )
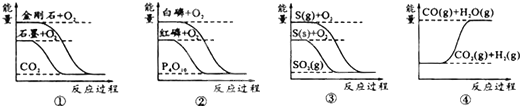

| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、CO (g)+H2O (g)=CO2 (g)+H2 (g)△H<0 |
| D、S (g)+O2 (g)=SO2 (g)△H1; S (s)+O2 (g)=SO2 (g)△H2,则△H1>△H2 |
 ③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中: