题目内容
已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.O×10-6 mol?L-l,c(PO43-)=1.58×10-6mol?L-l,则Ca3(PO4)2的Ksp为( )
| A、2.0×10-29 |
| B、3.2×l0-12 |
| C、6.3×10-18 |
| D、5.1×10-27 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:Ksp[Ca3(PO4)2]=[c(Ca2+)]3×[c(PO43-)]2,据此计算.
解答:
解:Ksp[Ca3(PO4)2]=[c(Ca2+)]3×[c(PO43-)]2=(2.O×10-6)3×(1.58×10-6)2=2.0×10-29,故选A.
点评:本题考查了沉淀的溶度积的计算,题目难度不大.

练习册系列答案
相关题目
下列分离和提纯的实验,所选用的方法和仪器不正确的是( )
| 序号 | A | B | C | D |
| 实验目的 | 食盐水与泥沙分离 | 制取蒸馏水 | 分离水和植物油 | 从浓食盐水中 得到氯化钠晶体 |
| 分离方法 | 萃取 | 蒸馏 | 分液 | 蒸发 |
| 选用仪器 | 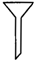 | 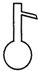 | 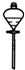 |  |
| A、A | B、B | C、C | D、D |
化学与科技、社会、生产有密切联系,下列说法正确的是( )
| A、氮化硅陶瓷、光导纤维均属于新型有机高分子材料 |
| B、用有机分子和C60制成“纳米车”,说明人类操纵分子技术已进入新阶段 |
| C、建筑材料ETFE为四氟乙烯与乙烯反应的共聚物,因此ETFE为纯净物 |
| D、光化学烟雾的产生与氮氧化物无关,因此氮氧化物可以任意排放 |
用惰性电极电解饱和Na2CO3溶液,若保持温度不变,则一段时间后( )
| A、溶液的酸性增强 | ||
B、c(Na+)与c(CO
| ||
| C、溶液浓度变大,有晶体析出 | ||
| D、溶液浓度不变,有晶体析出 |
北京奥运会“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述错误的是( )
| A、分子中的3个碳原子在一条直线上 |
| B、在光照条件下能和氯气发生取代反应 |
| C、充分燃烧的产物是水和二氧化碳 |
| D、丙烷和丁烷互为同系物 |
衡量一个国家化学工业发展水平标志的是下列哪一种物质的产量( )
| A、钢铁 |
| B、石油和煤 |
| C、乙烯 |
| D、CO2的排放量 |
随着人们生活水平的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要的原因是( )
| A、回收电池外壳的金属材料 |
| B、回收其中石墨电极 |
| C、不使电池中渗泄的电解液腐蚀其它物品 |
| D、防止电池中汞、镉等重金属离子对土壤和水源的污染 |