题目内容
【题目】随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精度也越来越高。现有一种简单可行的测定方法,具体步骤为:
①准确称取mg干燥后的NaCl固体细粒并转移到定容仪器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度,
计算出NaCl固体的体积V cm3。
(1)步骤①中仪器A最好使用_______________(填序号)
A.量筒 B.烧杯 C.容量瓶 D.试管
(2)步骤②中是否用酸式滴定管还是用碱式滴定管_____________,理由是__________。
(3)能否用水代替苯_________,理由是_____________________。
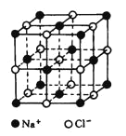
(4)已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm(如图),则用上述方法测得的阿伏加德常数NA的表达式为_______________。
【答案】(1)C (2)酸式滴定管;碱式滴定管的橡皮管会溶于苯而变形
(3)不能;水会溶解NaCl,不能测出NaCl固体的体积 (4)NA=![]()
【解析】
试题(1)定容容器为容量瓶,具有一定体积并便于振荡,所以C正确。
(2)苯具有腐蚀性,易腐蚀碱式滴定管中的橡皮管,只能用酸式滴定管。
(3)测量mgNaCl固体的体积,所加溶剂不能溶解NaCl,否则无法测出NaCl的体积,所以不能用水,应用苯。
(4)NaCl的密度为![]() ,NaCl晶胞的体积为(2a)3cm3,则NaCl晶胞的质量为
,NaCl晶胞的体积为(2a)3cm3,则NaCl晶胞的质量为![]() ×(2a)3cm3=
×(2a)3cm3=![]() ,一个NaCl晶胞含4个“NaCl”,而每个“NaCl”的质量为
,一个NaCl晶胞含4个“NaCl”,而每个“NaCl”的质量为![]() ,即
,即![]() =4×
=4×![]() ,解得NA=
,解得NA=![]() 。
。

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目