题目内容
7.下列离子方程式正确的是( )| A. | 铁片与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 二氧化硅和氢氧化钠溶液反应:SiO2+2OH-═SiO${\;}_{3}^{2-}$+H2O | |
| C. | 碳酸钡和稀硝酸反应:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| D. | 铜和氯化铁溶液反应:Fe3++Cu═Fe2++Cu2+ |
分析 A、铁和盐酸反应生成氯化亚铁;
B、二氧化硅和氢氧化钠溶液反应生成硅酸钠和水;
C、碳酸钡难溶于水,不能拆;
D、铜和氯化铁反应生成氯化亚铁和氯化铜.
解答 解:A、铁和盐酸反应生成氯化亚铁,故离子方程式为Fe+2H+═Fe2++H2↑,故A错误;
B、二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,其中二氧化硅和水不能拆,氢氧化钠和硅酸钠分别是强碱和可溶性盐,能拆,故离子方程式为SiO2+2OH-═SiO32-+H2O,故B正确;
C、碳酸钡难溶于水,不能拆,故离子方程式为BaCO3+2H+═CO2↑+H2O+Ba2+,故C错误;
D、铜和氯化铁反应生成氯化亚铁和氯化铜,离子方程式应满足电荷守恒,故离子方程式为2Fe3++Cu═2Fe2++Cu2+,故D错误.
故选B.
点评 本题考查了离子方程式书写的正误判断,难度不大,应注意离子方程式应满足电荷守恒、质量守恒等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某气态烃1mol能和2molHCl完全加成,加成后产物分子上的氢原子又可被6molCl2所取代,则此气态烃可能是( )
| A. | CH≡CCH3 | B. | CH2=CH2 | C. | CH≡CH | D. | CH2=C(CH3)2 |
20.能正确表示下列反应的离子方程式为( )
| A. | NaClO和NaOH的混合溶液中通入少量的SO2:ClO-+H2O+SO2=C1-+SO42-+2H+ | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O | |
| C. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| D. | 大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
15.下列混合物用加热的方法可分离的是( )
| A. | 氯化铵和氢氧化钙 | B. | 碘和氯化铵 | ||
| C. | 氯化铵和氯化钠 | D. | 氯化铵和碳酸氢钠 |
2.下列关于苯的说法中,正确的是( )
| A. | 苯的分子式是C6H6,不能使酸性高锰酸钾溶液褪色,属于饱和烃 | |
| B. | 从苯的凯库勒式看,分子中含有双键,所以苯属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴发生取代反应生成溴苯 | |
| D. | 苯泄露会导致苯溶入水中,渗入土壤,对周边农田、水源造成严重的污染 |
12.下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
| A. |  实验室用乙醇制取乙烯 | B. |  实验室制取乙酸乙酯 | ||
| C. |  分离苯和甲苯 | D. |  实验室制取硝基苯 |
19.根据下列实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加盐酸 | 有白色胶状沉淀生成 | 非金属性:Cl>Si |
| B | 向MnO2中滴入浓盐酸 | 有黄绿色气体产生 | 氧化性:MnO2>Cl2 |
| C | 向A溶液中滴加硝酸,再滴加KSCN溶液 | 溶液变成红色 | A溶液中一定有Fe3+ |
| D | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白质发生盐析 |
| A. | A | B. | B | C. | C | D. | D |
16.枸椽酸乙胺嗪可用于驱除肠道虫病,其结构简式为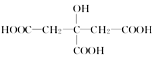 ,下列物质中不能与枸椽酸乙胺嗪反应的是( )
,下列物质中不能与枸椽酸乙胺嗪反应的是( )
 ,下列物质中不能与枸椽酸乙胺嗪反应的是( )
,下列物质中不能与枸椽酸乙胺嗪反应的是( )| A. | 乙酸 | B. | 乙醇 | C. | 溴的苯溶液 | D. | 氢氧化钠溶液 |
17.向物质M的溶液中逐滴加入HCl溶液,先产生白色沉淀,然后沉淀逐渐溶解,则物质M 可能是( )
| A. | MgSO4 | B. | AlCl3 | C. | NaAlO2 | D. | FeCl3 |