题目内容
5.下列化合物,按其晶体的熔点由高到低排列正确的是( )| A. | SiO2 CaO NaCl CBr4 CF4 | |
| B. | SiO2 NaCl CaO CF4 CBr4 | |
| C. | CaO NaCl SiO2 CBr4 CF4 | |
| D. | CF4CBr4NaCl CaO SiO2 |
分析 不同晶体的熔点:一般为原子晶体>离子晶体>金属晶体>分子晶体;相同晶体从影响晶体熔沸点高低的因素分析.
解答 解:SiO2为原子晶体,CaO和NaCl 为离子晶体,离子键与离子半径和离子所带电荷有关,离子半径越大和离子所带电荷越小,离子键越弱,熔点越小,半径Ca2+>Na+,Cl->O2-,所以NaCl的离子键最弱,熔点最低,而不同晶体的熔点:一般为原子晶体>离子晶体>金属晶体>分子晶体,
则SiO2熔点最高,其次为CaO>NaCl,CBr4和CF4都为分子晶体,分子的相对分子质量越大,分子间作用力越强,熔点越高,
则熔点:CBr4>CF4,
固有:SiO2>CaO>NaCl>CBr4>CF4,
故选A.
点评 本题考查晶体的类型与熔沸点的比较,题目难度不大,解答该类题目时要首先判断晶体的类型,晶体类型相同时,要注意晶体结构是否相似,把握影响晶体熔沸点的因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.某学生的实验报告所列出的下列数据中合理的是( )
| A. | .用10mL量筒量取7.28mL稀盐酸 | |
| B. | .用托盘天平称量25.50g NaCl | |
| C. | 用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.60mL | |
| D. | 用广泛pH试纸测得某溶液的pH为2.7 |
13.下列有关物质性质的说法正确的是( )
| A. | 硫是一种黄色晶体,易溶于水 | |
| B. | 钠是一种银白色金属,熔点较高,硬度较大 | |
| C. | 二氧化硫是一种无色、无味的有毒气体 | |
| D. | 二氧化氮石红棕色、有刺激性气味的有毒气体 |
17.下列各组物质是按化合物、单质、混合物顺序排列的是( )
| A. | 烧碱、液态氧、碘酒 | B. | 生石灰、白磷、熟石灰 | ||
| C. | 干冰、铁、氯化氢 | D. | 纯碱、氮气、氧气 |
14.用自来水养鱼之前,应先将盛有自来水的鱼缸放在阳光下晒一段时间,主要目的是( )
| A. | 除去水中的HClO | B. | 紫外线杀菌消毒 | C. | 增加水中含氧量 | D. | 提高水温 |
15.某化学反应的能量变化如图所示.下列有关叙述正确的是( )
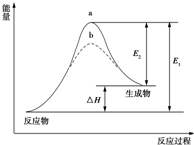

| A. | 该反应的反应热△H=E2-E1 | B. | 该反应为放热反应 | ||
| C. | 催化剂能改变反应的活化能 | D. | 催化剂能改变反应的焓变 |