��Ŀ����
��֪�����Ȼ�ѧ����ʽ��Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)
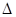 H=-24.8
kJ��mol-1
H=-24.8
kJ��mol-1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)
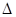 H=-47.2 kJ��mol-1
H=-47.2 kJ��mol-1
Fe3O4(s)+CO(g)=3FeO
(s)+CO2(g) 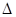 H=+640.5 kJ��mol-1
H=+640.5 kJ��mol-1
��14g CO����������FeO��ַ�Ӧ�õ�Fe���ʺ�CO2����ʱ�ķ�Ӧ��Ϊ�� ��
A��-218 kJ��mol-1 B��-109kJ��mol-1 C��+218 kJ��mol-1 D��+109 kJ��mol-1
���𰸡�
B
�����������ݢ�Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ��H����24.8 kJ/mol
��3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) ��H����47.2 kJ/mol
��Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) ��H����640.5 kJ/mol
�ɢ١�3���ڣ��ۡ�2�ɵ��Ȼ�ѧ����ʽΪ��
CO(g)+FeO(s)= Fe(s) + CO2(g) ��H= ��218.00 kJ/mol���ʴ�ΪB

��ϰ��ϵ�д�
�����Ŀ
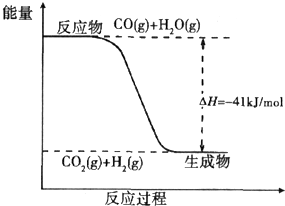 ú̿����ת��Ϊ�����Դ�ͻ���ԭ�ϣ�
ú̿����ת��Ϊ�����Դ�ͻ���ԭ�ϣ�